COVID-19-diagnostiikka pandemian jatkuessa
Koronan diagnosoimiseen käytettävien PCR-testien rinnalle on otettu käyttöön antigeenitestejä. Virusmuunnoksia etsitään sekvensoinnilla. Mikä on koronadiagnostiikan ajan henki ja miten rokotteiden tulo vaikuttaa?
Uuden koronaviruksen, SARS-CoV-2:n aiheuttamien infektioiden torjumiseksi tehdyt rajoitustoimet ovat olleet ennennäkemättömiä. Myös testausmäärät taudin havaitsemiseksi ovat epidemian jatkuessa kasvaneet huimiksi. Testaus on yksi lenkki ketjussa, jolla varmistetaan tartunnan saaneiden tunnistaminen, eristäminen ja karanteeniin määrääminen, altistuneiden kartoittaminen sekä tartuntaketjujen katkaiseminen (1).
Tässä artikkelissa päivitetään Lääkärilehdessä 24–33/2020 julkaistu artikkeli COVID-19-diagnostiikasta (2).
PCR-testit akuuttiin diagnostiikkaan
Luotettavin testi akuutin infektion osoittamiseksi on spesifinen nukleiinihapon osoittamiseen perustuva PCR-testi (3). Suomessa on tätä kirjoitettaessa tehty yli 3 miljoonaa testiä ja positiivinen tulos on saatu lähes 50 000 tapauksessa.
Testiä tehdään kaupallisilla PCR-testeillä sekä omavalmistuksena (in-house) toimiluvallisissa kliinisen mikrobiologian laboratorioissa. Tämän lisäksi käytössä on ns. pika-PCR-testejä (point of care, POC).
PCR-testien rinnalle on otettu käyttöön antigeeninosoitustestejä (4). Niiden etu on nopeus ja mahdollisuus tehdä testi keskuslaboratorion ulkopuolella. Haittapuolena on PCR-testiin verrattuna huonompi herkkyys. Lisäksi tiedetään, että virheellisten negatiivisten tulosten lisäksi voi esiintyä vääriä positiivisia löydöksiä. Antigeenitestituloksen varmistamisesta erilaisissa epidemiologisissa tilanteissa on ohjeistettu (4).
Näytteenoton haasteita
Näytteenotossa on haasteensa sekä PCR- että antigeenitestien käytettäessä. Näytteenoton ajoitus optimaaliseen viruksen erittymisaikaan on niistä yksi. Ei tarkkaan tiedetä, kuinka kauan ennen oireiden alkua virusta olisi PCR-testillä osoitettavissa.
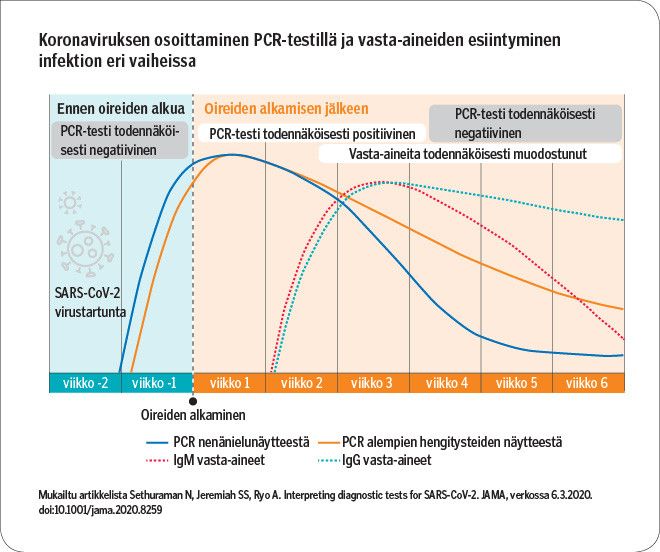
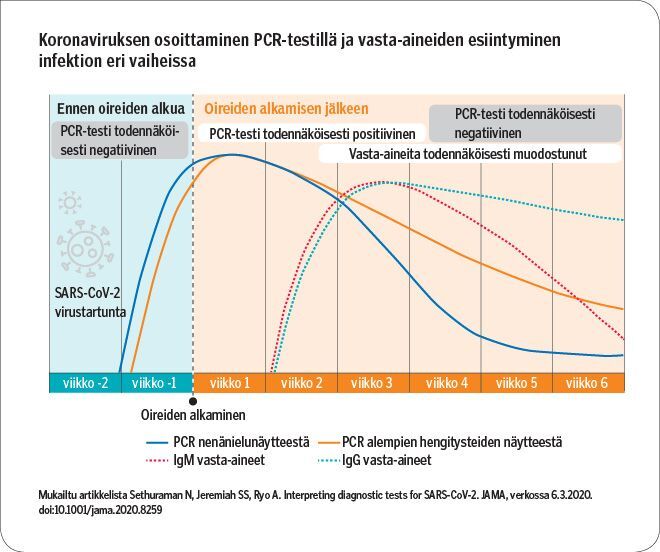
Nykytiedon mukaan viruseritys ja löytymistodennäköisyys PCR-testillä on suurimmillaan oireiden juuri alkaessa (kuvio). Virusta voidaan PCR-testillä osoittaa parhaimmillaan useita viikkoja oireiden alkamisesta. Kuitenkaan tällöin henkilöä ei enää pidetä tartuttavana, eikä lieväoireisen infektion jälkeen kontrollinäytteiden ottamista pidetä tarpeellisena. Antigeenitestille optimaalinen näytteenottoaika on 5 vrk oireiden alkamisesta tai 7 vrk altistumisesta.
Nenänielutikkunäyte on edelleen vallitseva näytemuoto. Nielunäytettä on myös Suomessa testattu, mutta sen herkkyys vaikuttaa heikommalta. Sylkinäytettä ei ole otettu laajemmin käyttöön.
Miten suhtautua negatiiviseen tulokseen?
Negatiivinen tulos kertoo siitä, että näytteenottohetkellä potilaalla ei käytetyllä analyysimenetelmällä voitu otetusta näytteestä osoittaa koronavirusta. Inkubaatioaika (1–14 vrk) on saattanut olla meneillään, mutta virus ei vielä näkynyt testissä. On myös mahdollista, että näytteenotto ei ole onnistunut ja tulos jää siksi negatiiviseksi.
Lisäksi potilaan oireiden ollessa alahengitysteissä ylähengitysteistä otettu näyte saattaa jäädä negatiiviseksi. Tällainen tilanne on tyypillisesti vakavaoireisella, sairaalahoitoa tarvitsevalla potilaalla. Tällöin suositellaan näytteenottoa alahengitysteistä, esimerkiksi huuhtelunäytettä (BAL).
Väärien negatiivisten tulosten osuutta analyyseistä on vaikeaa arvioida. Epäselvissä tilanteissa suositellaan uuden näytteen ottamista.
Rokotteen saaminen ei häiritse infektion toteamista PCR- tai antigeeninosoitustestillä.
Perimän sekvensoinnilla etsitään virusmuunnoksia
Koronaviruksen perimän emäsjärjestyksen määrittämisellä eli sekvensoinnilla voidaan tunnistaa muuntuneita viruskantoja. Tällä hetkellä seurataan erityisesti Britanniassa ensin todettua VOC 202012/01, 20B/501Y.V1 tai B.1.1.7 -viruskantaa ja Etelä-Afrikassa havaittua 20C/501Y.V2- tai B.1.351 -viruskantaa, joiden arvioidaan leviävän aiemmin havaittuja kantoja paremmin.
Suomessa on tällä hetkellä todettu yhteensä 232 muuntunutta koronaviruskantaa, joista 214 on brittivarianttia ja 18 Etelä-Afrikan varianttia.
Vasta-ainetestit tunnistavat sekä infektion että rokotteiden aikaansaamia vasta-aineita
Verinäytteestä tehtävällä vasta-ainetestillä voidaan osoittaa, esiintyykö näytteessä vasta-aineita SARS-CoV-2-virusta vastaan, ja siten arvioida, onko henkilö aiemmin saanut COVID-19-tartunnan. Vasta-aineita kehittyy keskimäärin kahden viikon viiveellä oireiden alkamisesta (kuvio), jolloin noin puolella tartunnan saaneista vasta-aineita on muodostunut.
Vasta-ainetesti näyttää positiivisen tuloksen vasta, kun infektio on jatkunut pidempään tai kun henkilö on jo parantunut. Tämän vuoksi vasta-ainetestit eivät sovellu akuutin taudin toteamiseen.
COVID-19-infektion saaneilla IgM-luokan vasta-aineita ei ole havaittavissa juurikaan IgG-vasta-aineita aikaisemmin, mutta IgG-vasta-aineiden pitoisuus suurenee pidempään ja pysyy suurentuneena pidempään.
Vasta-aineita voidaan mitata seerumi-, plasma- tai sormenpääverinäytteestä. Testit mittaavat vasta-aineita SARS-CoV-2-viruksen rakenneproteiineja eli antigeeneja vastaan. Tällainen antigeeni on esimerkiksi viruksen pinnan piikkiproteiini. Viruksen sisällä oleva nukleoproteiini on myös hyvin immunogeeninen eli aktivoi kyseisen rakenteen tunnistavia immuunipuolustuksen soluja. Useimmat kaupalliset vasta-ainetestit perustuvat joko viruksen piikkiproteiiniin, nukleoproteiiniin tai molempiin.
Vasta-ainetesteillä voidaan mitata paitsi infektion tuottamia, myös rokottamalla aikaansaatuja vasta-aineita. Useimmat kehitteillä olevat ja kaikki myyntiluvan saaneet koronavirusrokotteet perustuvat viruksen piikkiproteiiniin. Piikkiproteiinivasta-aineita mittaavalla testillä ei voida erottaa infektion ja rokotteen aikaansaamia vasta-aineita toisistaan. Vasta-ainetesteillä, jotka tunnistavat nukleoproteiinia kohtaan muodostuneita vasta-aineita, voidaan mitata infektion seurauksena muodostuneita vasta-aineita myös rokotteen saaneilla.
Koska vasta-ainetaso laskee ajan myötä, testin herkkyys vaikuttaa siihen, voidaanko aiempi tartunta tunnistaa siinä. Nukleoproteiinivasta-aineiden on nähty hiipuvan aikaisemmin tartuntaa seuraavien kuukausien aikana, kun taas piikkiproteiinivasta-ainetasot säilyvät koholla suuremmalla osalla pidempään. Testivalmistajat eivät aina ilmoita, mihin antigeeniin tai antigeenien yhdistelmään vasta-ainetesti perustuu.
Vasta-ainepikatestit ovat raskaustestin kaltaisia immunokromatografisia liuskatestejä, joissa näyte voidaan tutkia sormenpäästä otettavasta verinäytteestä, seerumi- tai plasmanäytteestä. Pikatestin tulos on luettavissa nopeasti. Laboratoriossa tehtävillä testeillä, kuten entsyymi-immunologisella eli ELISA-testillä, voidaan seerumi- tai plasmanäytteestä mitata vasta-aineiden määrää kvantitatiivisesti tai semikvantitatiivisesti. Kaupallisten vasta-ainetestien laadussa on paljon vaihtelua.
Neutraloivia vasta-aineita mittaavalla testillä voidaan luotettavimmin todeta COVID-19-infektion seurauksena muodostuneita vasta-aineita. Neutraloivat vasta-aineet estävät viruksen kiinnittymisen solun reseptoriin ja viruksen pääsemisen solun sisään. Virusta neutraloivat vasta-aineet kohdistuvat etenkin viruksen piikkiproteiineihin.
Yksittäinen vasta-ainetesti ei välttämättä riitä
Parittaisista akuutin ja toipilasvaiheen verinäytteistä on periaatteessa mahdollista tutkia vasta-aineiden lisääntymistä ja siten arvioida COVID-19-infektion mahdollisuutta tilanteessa, jossa taudinaiheuttaja on jäänyt selvittämättä.
Yksittäisestä verinäytteestä tehtävä vasta-ainetesti ei välttämättä anna luotettavaa tulosta silloin, kun taudinaiheuttajan yleisyys väestössä on vähäinen. Mitä harvinaisempi on todellisen positiivisen testituloksen mahdollisuus, sitä suurempi on väärän positiivisen tuloksen todennäköisyys. Edelleen vain pienellä osalla väestöstä on tartunnan seurauksena muodostuneita koronaviruksen vasta-aineita, eli seroprevalenssi Suomen väestössä on hyvin pieni, noin yhden prosentin ja Helsingin ja Uudenmaan sairaanhoitopiirin alueella kahden prosentin luokkaa (5).
Väärän tuloksen riskiin vaikuttaa myös testin suorituskyky eli herkkyys ja tarkkuus. Herkkyys tarkoittaa sitä, kuinka suuresta osasta infektion sairastaneiden henkilöiden näytteitä testi tunnistaa vasta-aineita. Tarkkuus tarkoittaa sitä, millä todennäköisyydellä testi antaa negatiivisen tuloksen näytteestä, kun henkilö ei ole sairastanut kyseistä infektiota.
Jos vasta-ainetestin tarkkuus on esimerkiksi 98 % ja väestön todellinen seroprevalenssi 0,5 %, testillä saaduista positiivisista tuloksista todennäköisesti kolme neljästä olisi vääriä. Tällöin testi voi tunnistaa esimerkiksi toisen koronavirusinfektion seurauksena muodostuneita vasta-aineita.
Suomen epidemiologisessa tilanteessa tartunnan seurauksena muodostuneita vasta-aineita mittaavat testit soveltuvat ensisijaisesti tutkimuskäyttöön, kun arvioidaan tartuntojen määrää väestössä tai tietyissä kohderyhmissä. Markkinoilla on myös hyvin tarkkoja laboratoriokäyttöön tarkoitettuja vasta-ainetestejä, joita voidaan joissain tapauksissa käyttää sen arvioimiseksi, onko henkilö aiemmin sairastanut COVID-19-infektion. Tuloksen luotettavuutta voidaan parantaa myös käyttämällä toista vasta-ainetestiä positiivisen tuloksen varmistamiseksi.
Vasta-aineet säilyvät pitkään
Tämänhetkisen tiedon perusteella lähes kaikille tartunnan saaneille muodostuu vasta-aineita, jotka säilyvät ainakin yli puolen vuoden ajan tartunnan jälkeen (6). Valtaosalle taudin sairastaneista muodostuu myös neutraloivia vasta-aineita, joilla todennäköisesti on merkitystä suojassa virustartuntaa vastaan.
Vasta-ainetestien perusteella ei kuitenkaan voida varmuudella päätellä, onko henkilö suojassa uudelta tartunnalta, eikä määrittää tartunnan ajankohtaa. Useissa tutkimuksissa on havaittu, että sairastetun taudin vakavuus voi vaikuttaa muodostuvan immuniteetin voimakkuuteen: lieväoireisessa infektiossa vasta-ainevaste jää heikommaksi ja siten vasta-aineiden määrä voi myös hiipua aikaisemmin. Toisaalta myös T-soluihin perustuva soluvälitteinen immuniteetti voi vaikuttaa suojaan.
- 1
- STM. Suomi lisää koronavirustestausta merkittävästi. https://stm.fi/artikkeli/-/asset_publisher/krista-kiuru-suomi-lisaa-koronavirustestausta-merkittavasti
- 2
- Savolainen-Kopra C, Melin M. COVID-19-diagnostiikka ja sen osuvuus. Suom Lääkäril 2020;75:1530–2.
- 3
- WHO. Molecular assays to diagnose COVID-19: Summary table of available protocols 24 January 2020-. https://www.who.int/who-documents-detail/molecular-assays-to-diagnose-covid-19-summary-table-of-available-protocols
- 4
- THL. Ohje antigeenitestien käytöstä koronavirusdiagnostiikassa. https://thl.fi/fi/web/infektiotaudit-ja-rokotukset/taudit-ja-torjunta/taudit-ja-taudinaiheuttajat-a-o/koronavirus-covid-19/koronaviruksen-covid-19-laboratoriotutkimukset/ohje-antigeenitestien-kaytosta-koronavirusdiagnostiikassa
- 5
- THL. THL alkaa julkaista väestötutkimuksen koronavirusvasta-ainetuloksia viikoittain. https://thl.fi/fi/-/thl-alkaa-julkaista-vaestotutkimuksen-koronavirusvasta-ainetuloksia-viikoittain
- 6
- THL. THL:n tutkimus: Valtaosalla koronavirustartunnan saaneista vasta-aineet säilyvät yli puolen vuoden ajan. https://thl.fi/fi/-/thl-n-tutkimus-valtaosalla-koronavirustartunnan-saaneista-vasta-aineet-sailyvat-yli-puolen-vuoden-ajan