Ulosteenkarkailu ja sen hoito sakraalisella neuromodulaatiolla
• Sakraalinen neuromodulaatio on vakiintunut hoitomuoto ulosteenkarkailuun.
• Hoitoon pääsy edellyttää, että potilas on käynyt läpi konservatiivisen hoidon. Ikä ei ole hoidon este.
• Eniten hoidosta hyötyvät potilaat, joilla on synnytyksen yhteydessä tullut sulkijalihasvaurio.
• Komplikaatiot ovat yleensä lieviä infektioita, ja vakavia komplikaatioita esiintyy harvoin.

Ulosteenkarkailusta kärsii tutkimusten mukaan 2–18 % länsimaiden aikuisväestöstä (1). Tampereella tehdyn tutkimuksen mukaan suomalaisessa aikuisväestössä esiintyvyys on noin 10,6 % (2,3). Vaivasta puhuminen on monelle hankalaa, ja niinpä todellinen potilasmäärä voi olla jopa suurempi.
Ulosteenkarkailun hoito on pitkälti konservatiivinen, riippumatta karkailun vaikeusasteesta ja syystä. Sakraalihermon stimulaatio eli sakraalinen neuromodulaatio (SNM) on suhteellisen uusi menetelmä ulosteenkarkailun hoidossa. Se kehitettiin ensin virtsankarkailuun, mutta pian sen huomattiin tehoavan myös muihin lantionpohjan ongelmiin, kuten ulosteenkarkailuun.
Ensimmäisen sakraalihermon toimintaan vaikuttavan tahdistimen asensivat urologit Schmidt ja Tanagho vuonna 1982 Kaliforniassa (4). Vuonna 1994 annettiin ensimmäiselle sakraaliselle neuromodulaatiolaitteelle eurooppalainen CE-merkki ja laite hyväksyttiin käytettäväksi virtsankarkailun hoitoon. Virallinen hyväksyntä laitteen käytölle ulosteenkarkailun hoidossa seurasi vuonna 2010.
Suomen ensimmäinen sakraalinen neuromodulaatio tehtiin vuonna 1996 Oysissa virtsankarkailun takia. Vuonna 1999 asennettiin ensimmäinen sakraalinen neuromodulaattori ulosteenkarkailupotilaalle. Siitä lähtien Suomessa on hoidettu neuromodulaatiolla 80–100 ulosteenkarkailupotilasta vuodessa (5).
Ulosteenkarkailun esiintyvyys ja syyt
Noin 70 % ulosteenkarkailusta kärsivistä on naisia. Vaivalle altistavat alatiesynnytys ja raskaus.
Ulosteenkarkailun taustalla voi olla akuutti infektioripuli, ulostuslääkkeiden väärinkäyttö tai peräsuolen kasvain. Harvinaisempia sulkijalihasvaurion syitä ovat peräaukon seutuun kohdistuvat leikkaukset, kuten fisteli-, peräpukama- ja peräsuolisyöpäkirurgia. Myös peräaukon seutuun kohdistuvat vammat voivat aiheuttaa sulkijalihasvaurion (3,6) (taulukko 1).
Ulosteenkarkailun syynä voi olla myös hermovaurio, jonka vuoksi sulkijalihasten toimintakyky tai peräsuolen venytysaistin heikentyy.
Raskaus ja alatiesynnytys altistavat lantionpohjan elimien, erityisesti peräsuolen laskeuman ja sen seurauksena peräsuolen tuppeuman kehittymiselle. Tämä voi olla yhtenä syynä ulosteenkarkailun kehittymiseen (7,8). Pikkulantion elimien prolapsin syynä pidetään raskauden aikana pikkulantion alueelle kohdistuva painetta, joka johtaa peräsuolen ja muiden pikkulantion tukikudosten löystymiseen ja sitä myötä lantionpohjan elimien prolapsiin (9). Lisäksi pikkulantion alueen kirurgiset toimenpiteet, kuten kohdunpoisto, voivat altistaa peräsuolen prolapsille ja tuppeutumiselle.
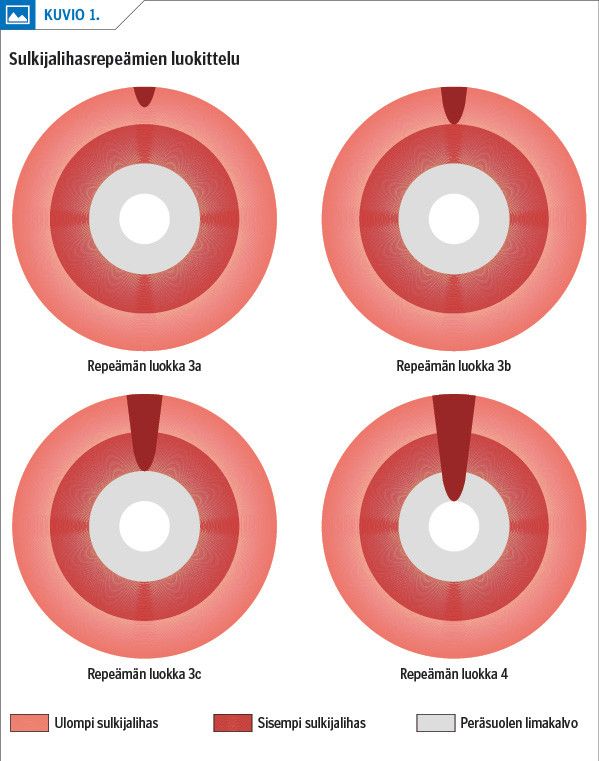
Alatiesynnytyksen yhteydessä tullut sulkijalihaksen repeämä voi myös olla ulosteenkarkailun taustalla (10). Repeämät luokitellaan syvyyden mukaan astekoilla 1–4 (kuvio 1) (11). Kolmannen asteen repeämä ulottuu sulkijalihaksiin, neljännen asteen repimässä on revennyt myös peräsuolen seinämä. Kolmannen ja neljännen asteen synnytysrepeämiä todetaan Suomessa THL:n tilastojen mukaan vuosittain noin 1,2 %:lla synnyttäjistä (12).
Vaikea ulosteenkarkailuongelma heti synnytyksen jälkeen on harvinainen (13). Valtaosalla potilaista karkailuoireet ovat aluksi lieviä, kuten tuhrimista ja ilman karkailua (14). Ajan mittaan lihasvoiman heikentyessä oireet pahenevat (15).
Tuoreimmat tutkimukset viittaavat siihen, että pikkulantion prolapsin riskitekijät ovat melkein samat kuin synnytyksen yhteydessä tulleen sulkijalihasvaurion: ensisynnytys, imukuppi- tai pihtisynnytys, isokokoinen sikiö, pitkä ponnistusvaihe, epiduraalipuudutus ja synnytyksen käynnistäminen lääkkeillä (9,16,17,18,19).
Sulkijalihasrepeämän välttämiseksi on kehitetty erilaisia välilihaa tukevia menetelmiä. Tutkituin niistä on Pirhosen vuonna 1998 kehittämä toimenpide, joka tunnetaan maailmalla suomalaisena manööverinä (the Finnish manouvre) (20).
Potilaan tutkiminen
Ulosteenkarkailupotilasta tutkiessa on erittäin tärkeää selvittää karkailun luonne. Ulostamisvaikeuksia valittavilta potilailta tulisi kysyä ulosteenkarkailusta. Perustutkimuksen yhteydessä selvitetään oireen kesto ja tiheys ja mitä karkaa (kova uloste tai ripuli). Samalla kysytään, onko tehty peräaukon tai selän alueen leikkauksia, mitä lääkkeitä on käytössä ja onko perussairauksia, kuten neurologisia sairauksia.
Oireiden vaikeusasteen selvittämistä helpottavat kyselylomakkeet, kuten Wexnerin oirekysely (taulukko 2). Siinä ulosteenpidätyskyvyn hankaluutta arvioidaan asteikolla 0–20 ja korkeampi pistemäärä merkitsee suurempaa haittaa. Mikäli pistearvo on yli 11, vaiva on vaikeasti elämänlaatua häiritsevä (21).
Oireen vaikeusastetta voidaan karkeasti arvioida VAS-asteikolla 1–10. Ulostamispäiväkirjan avulla voidaan selvittää, montako kertaa päivässä on tarve ulostaa sekä mikä on tuhrimisten ja karkailuvahinkojen määrä. Päiväkirjaa pitäisi pitää vähintään kaksi viikkoa.
Perustutkimukseen kuuluu myös peräaukon inspektio. Inspektiossa nähdään, onko peräaukko kiinni vai auki (prolapsi, tuppeuma tai sulkijalihasvaurio), välilihan pituus, mahdolliset arvet ja peräaukon ihon kunto. Ponnistuskokeessa potilas istuu pytyllä ja ponnistaa samalla tavoin kuin ulostaessa. Jos perineum laskee alle istuinkyhmytason, voidaan nähdä lantionpohjan laskema, peräsuolen prolapsi tai emättimen tai kohdun laskeuma.
Tuseerauksella arvioidaan sulkijalihaksen tonus sekä levossa että jännitettäessä. Tarkistetaan, tuntuuko haavaumia tai kasvaimia. Proktoskopiassa voidaan nähdä peräpukamat, peräaukon haavauma, peräsuolen tuppeutuminen ja prolapsi. Kolonoskopialla voidaan sulkea pois tulehdukselliset suolisairaudet ja kasvaimet.
Peräaukon paineenmittauksella voidaan tutkia sulkijalihasten toimintaa. Sisempi sulkijalihas on sileää lihasta, eikä sitä voi tahdonalaisesti supistaa. Paineenmittauksessa mitattu lepopaine kuvaa sisemmän sulkijalihaksen toimintaa. Ulompi sulkijalihas on pääosin poikkijuovaista lihasta, ja sitä voi supistaa tahdonalaisesti. Paineenmittauksessa peräaukon supistusvoima kertoo ulomman sulkijalihaksen toiminnasta (22). Anaalimanometrialla voidaan selvittää myös peräsuolen tunnistuskyky ja laajentumisherkkyys, joka antaa viitteitä hermojen toiminnasta (23).
Peräaukon kautta tehtävällä kaikututkimuksella voidaan tarkistaa, ovatko sulkijalihakset ehjät. Kokenut proktologi voi tehdä sen vastaanoton yhteydessä. Toimenpide on nopea ja kivuton eikä vaadi etukäteisvalmisteluja. Nykyään peräaukon sulkijalihasrepeämä voidaan todeta yhtä luotettavasti myös magneettikuvauslaitteilla (24).
Defekografialla voidaan selvittää pikkulantion elimien ja peräsuolen prolapsin vaikeusaste. Tässä tutkimuksessa laitetaan varjoainetta potilaan peräsuoleen, emättimeen ja sitä annetaan myös suun kautta. Sen jälkeen ulostamistapahtuma kuvataan.
Konservatiivinen hoito
Ulosteenkarkailupotilaan hoito on ensisijaisesti konservatiivinen ja se voidaan toteuttaa perusterveydenhuollossa. Hoidon kulmakivi ovat kuituvalmisteet. Ne tasoittavat suolen toimintaa ja vähentävät ripulia (25), ja niiden on osoitettu vähentävän merkittävästi karkailuepisodeja.
Ylivuotoinkontinenssia voidaan alkuvaiheessa hoitaa peräruiskein. Lääkehoitoa voi tarvittaessa tehostaa sisemmän sulkijalihaksen voimaa ja suolen toimintaa hidastavilla lääkkeillä (loperamidi). Annos on yksilöllinen, alkuannos on 2 mg ja sitä voidaan suurentaa aina 16 mg:aan/vrk (26). Osa potilaista hyötyy myös anaalitamponeista.
Pelkkä fysioterapia ei ole osoittautunut tehokkaaksi ulosteenkarkailun hoidossa, mutta yhdessä kuituvalmisteiden ja biopalautehoidon kanssa siitä on apua (27,28,29). Suolihuuhtelulla voidaan tyhjätä peräsuoli ja paksusuolen loppuosa ulosteesta, jolloin liikkuminen on vapaampaa. Opetusta suolihuuhteluun saa sairaalassa siihen perehtyneeltä sairaanhoitajalta (30).
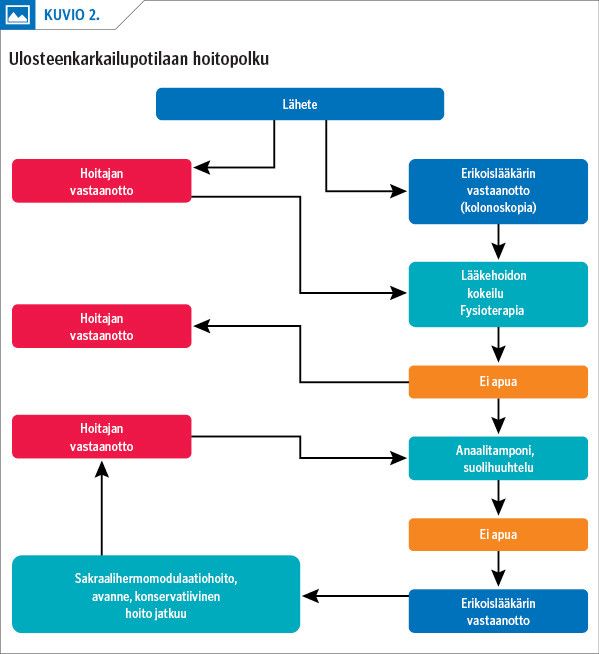
Konservatiivinen hoito on yleensä tehokas ja potilaat voi pärjätä vuosia ilman mitään invasiivisempia toimenpiteitä (3,31). Esimerkki ulosteenkarkailupotilaiden hoitopolusta Seinäjoen ja Vaasan keskussairaaloissa sekä Turun yliopistollisessa keskussairaalassa on esitetty kuviossa (kuvio 2).
Kirurginen hoito
Mikäli konservatiivinen hoito ei auta ulosteenkarkailuun, on harkittava kirurgisia toimenpiteitä. Tavallisimmat ovat lantionpohjan laskeuman korjaus rektopeksialla, sakraalihermomodulaatio, sulkijalihaksen korjausleikkaus ja avanne. Peräsuolen tuppeumaan tai prolapsiin liittyvä ulosteenkarkailu voidaan hoitaa peräsuolen ripustusleikkauksella (32). Verkolla tehtävä peräsuolen ripustusleikkaus on kotimaisessa tutkimuksessa osoittautunut tehokkaaksi erityisesti ulkoisen prolapsin hoidossa (33).
Peräaukon sulkijalihasten rakenne voidaan tarkistaa kaikututkimuksella tai lantion magneettikuvauksella (24). Mikäli niissä todetaan sulkijalihasrepeämä eikä konservatiivinen hoito ole auttanut, voidaan yrittää vielä uusintakorjausleikkausta (34). Nuorille naisille leikkaus kannattaa tehdä pian synnytyksen jälkeen (35,36). Jos kuvantamistutkimuksissa todetaan repeämä, mutta siitä ei ole oireita, jatketaan fysioterapiaa ja omatoimista harjoittelua lantionpohjan lihasten vahvistamiseksi.
Iäkkäillä potilailla sulkijalihaksen korjausleikkauksen tulokset ovat huonot (35,37).
Ellei kirurginen, konservatiivinen tai sakraalinen neuromodulaatiohoito tehoa karkailuun, on vaihtoehtona on tehdä avanne, jos potilas sen haluaa.
Sakraalinen neuromodulaatio
Mikäli konservatiivinen hoito tai muut toimenpiteet ei tuota toivottua tulosta, voidaan harkita sakraalista neuromodulaatiota. Sen vaikutusmekanismi on edelleen epäselvä, mutta todennäköisesti vaikutus perustuu sakraalisessa hermojuuressa olevien afferenttien tuntosäikeiden ärsytyksen kautta tapahtuviin aivokuoren oppimiskeskusten muutoksiin (38).
Neuromodulaatiolaitteen kanssa selviytyminen edellyttää potilaalta älypuhelimen tyyppisen laitteen käyttöä, kykyä antaa palautetta hoidon tehosta ja käsien käyttöä. Ikä ei ole este, mutta heikko liikuntakyky ja muistisairaus ovat. Lisäksi on tärkeää arvioida potilaan psyykkinen tila ja hoitoon kohdistuvat odotukset. Raskauden ajaksi neuromodulaattori on suljettava.
Neuromodulaattorihoidon alkukustannukset ovat varsin korkeat, joten hoito on rajattava niille, jotka sitä eniten hyötyvät.
Hoidon toteutus
Sakraalinen neuromodulaatio on kevyt ja varsin turvallinen päiväkirurginen toimenpide. Siinä potilaalle asennetaan elektrodi S3- tai S4-hermojuuren viereen paikallispuudutuksessa leikkaussalissa. Elektrodin oikea sijainti varmistetaan läpivalaisussa.
Ensimmäiset 2–3 viikkoa elektrodi on yhdistettynä väliaikaiseen ulkoiseen tahdistimen. Potilas pitää oirepäiväkirjaa ennen tahdistimen asentamista, väliaikaisen tahdistimen ollessa päällä ja koejakson loppumisen aikana, tahdistimen ollessa sammutettu. Mikäli koejakson aikana ulosteenkarkailutapahtumat vähenevät vähintään 50 % ja tahdistimen ollessa sammutettu oireet palaavat, voidaan asentaa pysyvä tahdistin.
Pysyvä tahdistin tunneloidaan ihoalaiskudokseen pakaraan seutuun. Laite muistuttaa ulkonäöltään sydämentahdistinta. Sen akku kestää noin viisi vuotta. Markkinoilla on myös ladattava versio sekä magneettikuvauslaitteen kanssa yhteensopiva laite.
Oirekyselyt, kuten Wexnerin pisteytys, VAS-mittaus ja ulostuspäiväkirja, helpottavat hoidon tarpeen ja jatkossa sen tehokkuuden arvioimista.
Komplikaatiot
Sakraalisen neuromodulaation yleisin komplikaatio on kipu tahdistimen tai elektrodin seudussa. Leikkausalueen tulehdusriskin pienentämiseksi suositellaan antibioottiprofylaksiaa. Tahdistin tai elektrodi joudutaan poistamaan komplikaation takia alle 2 %:lta potilaista (39).
Suomalaisessa aineistossa komplikaatioita esiintyi noin 15 %:lla potilaista. Tavallisin oli leikkausalueen kipu (5).
Tulokset Suomessa
Vuonna 2018 julkaistussa suomalaisessa tutkimuksessa selvitettiin sakraalisen neuromodulaatiohoidon kansalliset tulokset vuosilta 1999–2017. Tutkimukseen kerättiin takautuvasti tiedot potilaista, joille toimenpide oli tehty vatsaelinkirurgisin perustein. Tavallisimmat syyt olivat ulosteenkarkailu (n = 452), lantionpohjan kivut tai endometrioosi (n = 52) ja ummetus (n = 133).
Parhaiten toimenpide auttoi ulosteenkarkailupotilaita: heistä 59 % oli hoitotulokseen tyytyväisiä keskimäärin 2,4 vuoden seurannan jälkeen.
Ulosteenkarkailun syy vaikutti hoidon onnistumiseen. Eniten hoidosta hyötyivät potilaat, joilla ulosteenkarkailun aiheutti synnytysvaurio, sekä potilaat, joiden ulosteenkarkailun syy ei ollut tiedossa. Huonoiten hoito auttoi leikkauksenjälkeisessä ulosteenkarkailussa, kuten peräsuolisyöpäleikkausten jälkeen (5).
Samasta aineistosta selvitettiin myös, miten sulkijalihasvaurio vaikuttaa hoidon onnistumiseen, vertaamalla potilaita, joilla kaikututkimuksessa oli korjaamaton sulkijalihasvaurio, ja potilaita, joiden sulkijalihasvaurio oli aiemmin korjattu. Sulkijalihasvaurio ei vaikuttanut hoidon tulokseen. Sakraalisen neuromodulaatiohoidon onnistuminen ei siis edellytä edeltävää sulkijalihasten korjausleikkausta (37).
Pitkäaikaistulokset
Osa potilaista ei välttämättä hyödy riittävästi sakraalisesta hermomodulaatiosta. Koska hoidon tehokkuutta on hankalaa arvioida etukäteen, sitä testataan väliaikaisella tahdistimella ennen pysyvän laitteen asettamista.
Niukka tutkimusnäyttö osoittaa, että eniten hoidosta hyötyvät potilaat, joilla ulosteenkarkailu johtuu synnytysvauriosta. Näiden potilaiden koejakson tulokset sekä pitkäaikaistulokset ovat paremmat kuin potilailla, joilla ulosteenkarkailu johtui muista syistä (5).
Mikäli koejakso onnistuu ja potilas saa pysyvän tahdistimen, pitkäaikaistulokset ovat hyvät. Suuressa eurooppalaisessa monikeskustutkimuksessa osoitettiin, että pysyvän tahdistimen saaneista noin 86 % oli tyytyväisiä hoidon tulokseen viiden vuoden kuluttua (40).
Tarja Pinta: EVO-rahoitus.
Jaan Kirss: Valtion tutkimusrahoitus laitoksella.
- 1
- Sharma A, Yuan L, Marshall RJ, Merrie AE, Bissett IP. Systematic review of the prevalence of faecal incontinence. Br J Surg 2016;103:1589–97.
- 2
- Aitola P, Lehto K, Fonsell R, Huhtala H. Prevalence of faecal incontinence in adults aged 30 years or more in general population. Colorectal Dis 2010;12:687–91.
- 3
- Saldana Ruiz N, Kaiser AM. Fecal incontinence - Challenges and solutions. World J Gastroenterol 2017;23:11–24.
- 4
- Tanagho E, Schmidt R. Bladder pacemaker: Scientific basis and clinical future. Urology 1982;20:614–9.
- 5
- Kirss J, Pinta T, Varpe P ym. Outcomes of treatment of faecal incontinence with sacral nerve stimulation - a Finnish multicentre study. Colorectal Dis 2019;21:59–65.
- 6
- Hayden DM, Weiss EG. Fecal incontinence: etiology, evaluation, and treatment. Clin Colon Rectal Surg 2011;24:64–70.
- 7
- Yagi Y, Tsunoda A, Takahashi T, Kusanagi H. Rectoanal intussusception is very common in patients with fecal incontinence. J Anus Rectum Colon 2018;2:162–7.
- 8
- Gosselink MP, Joshi HM. Exploring the link between high grade internal rectal prolapse and faecal incontinence. Colorectal Dis 2017;19:711–2.
- 9
- Cattani L, Decoene J, Page AS, Weeg N, Deprest J, Dietz HP. Pregnancy, labour and delivery as risk factors for pelvic organ prolapse: a systematic review. Int Urogynecol J 2021;32:1623–31.
- 10
- Ditah I, Devaki P, Luma HN ym. Prevalence, trends, and risk factors for fecal incontinence in United States adults, 2005-2010. Clin Gastroenterol Hepatol 2014;12:636–43 e1-2.
- 11
- Sultan A. Obstetrical perineal injury and anal incontinence. Pääkirjoitus. Clinical Risk 1999;5:193–6.
- 12
- Laine K, Gissler M, Pirhonen J. Changing incidence of anal sphincter tears in four Nordic countries through the last decades. Eur J Obstet Gynecol Reprod Biol 2009;146:71–5.
- 13
- Pinta T, Kylänpää M, Teramo K, Luukkonen P. Sphincter rupture and anal incontinence after first vaginal delivery. Acta Obstet Gynecol Scand 2004;83:917–22.
- 14
- Sundquist J. Long-term outcome after obstetric injury: a retrospective study. Acta Obstet Gynecol Scand 2012;91:715–8.
- 15
- Pinta T. Anal incontinence and anal sphincter rupture during childbirth. Väitöskirja 2005.
- 16
- Thomas V, Shek KL, Guzman Rojas R, Dietz HP. Temporal latency between pelvic floor trauma and presentation for prolapse surgery: a retrospective observational study. Int Urogynecol J 2015;26:1185–9.
- 17
- Kapaya H, Hashim S, Jha S. OASI: a preventable injury? Eur J Obstet Gynecol Reprod Biol 2015;185:9–12.
- 18
- Drusany Staric K, Bukovec P, Jakopic K, Zdravevski E, Trajkovik V, Lukanovic A. Can we predict obstetric anal sphincter injury? Eur J Obstet Gynecol Reprod Biol 2017;210:196–200.
- 19
- Levin G, Rottenstreich A, Tsur A ym. Risk factors for obstetric anal sphincter injury among parous women. Arch Gynecol Obstet 2021;303:709–14.
- 20
- Pirhonen J, Grenman S, Haadem K ym. Frequency of anal sphincter rupture at delivery in Sweden and Finland – result of difference inmanual help to the baby’s head. Acta Obstet Gynecol Scand 1998;77:974–7.
- 21
- Jorge J, Wexner S. Etiology and management of fecal incontinence. Dis Colon Rectum 1993;36:77–97.
- 22
- Corsetti M, Passaretti S, Barzaghi F, Missale G. Anorectal manometry with water-perfused catheter in healthy adults with no functional bowel disorders. Colorectal Dis 2010;12:220–5.
- 23
- Pedersen I, Christiansen J. A study of the physiological variation in anal manometry. Br J Surg 1989;76:69–70.
- 24
- Kirss J, Pinta T, Victorzon S, Kallio-Packalén M, Victorzon M. External phased-array magnetic resonance imaging in the diagnosis of obstetric anal sphincter injury- a pilot study. ESCP 11th Scientific meeting, Milan: Turku University Hospital; 2016.
- 25
- Bliss D, Jung H, Savik K ym. Supplementation with dietary fiber improves fecal incontinence. Nursing Research 2001;50:203–13.
- 26
- Omar MI, Alexander CE. Drug treatment for faecal incontinence in adults. Cochrane Database Syst Rev 2013.
- 27
- Norton C, Cody J. Biofeedback and/or sphincter exercises for the treatment of faecal incontinence in adults. Cochrane Database Syst Rev 2012.
- 28
- Sjödahl J, Walter SA, Johansson E, Ingemansson A, Ryn A-K, Hallböök O. Combination therapy with biofeedback, loperamide, and stool-bulking agents is effective for the treatment of fecal incontinence in women – a randomized controlled trial. Scand J Gastroenterol 2015;50:965–74.
- 29
- Woodley SJ, Boyle R, Cody JD, Mørkved S, Hay–Smith EJC. Pelvic floor muscle training for prevention and treatment of urinary and faecal incontinence in antenatal and postnatal women. Cochrane Database Syst Rev 2017;12(CD007471).
- 30
- Sturkenboom R, van der Wilt AA, van Kuijk SMJ ym. Long-term outcomes of a Malone antegrade continence enema (MACE) for the treatment of fecal incontinence or constipation in adults. Int J Colorectal Dis 2018;33:1341–8.
- 31
- Forte M, Andrade K, Butler M ym. Treatments for fecal incontinece. Agency for Healthcare Research and Quality 2016;15(16).
- 32
- Maeda K, Katsuno H, Tsunoda A ym. Japanese practice guidelines for fecal incontinence part 3 -surgical treatment for fecal incontinence, fecal incontinence in a special conditions- English version. J Anus Rectum Colon 2021;5:84–99.
- 33
- Makela-Kaikkonen J, Rautio T, Kairaluoma M ym. Does ventral rectopexy improve pelvic floor function in the long term? Dis Colon Rectum 2018;61:230–8.
- 34
- Andrews V, Sultan AH, Thakar R, Jones PW. Occult anal sphincter injuries--myth or reality? BJOG 2006;113:195–200.
- 35
- Pinta T, Kylänpää-Bäck M, Salmi T, Järvinen H, Luukkonen P. Delayed sphincter repair for obstetric ruptures: Analysis of failure. Colorectal Dis 2001;5:73–8.
- 36
- Barbosa M, Glavind-Kristensen M, Christensen P. Early secondary repair of obstetric anal sphincter injury: postoperative complications, long-term functional outcomes, and impact on quality of life. Tech Coloproctol 2020;24:221–9.
- 37
- Kirss J Jr., Pinta T, Rautio T ym. Impact of sphincter lesions and delayed sphincter repair on sacral neuromodulation treatment outcomes for faecal incontinence: results from a Finnish national cohort study. Int J Colorectal Dis 2018;33:1709–14.
- 38
- Lundby L, Moller A, Buntzen S ym. Relief of fecal incontinence by sacral nerve stimulation linked to focal brain activation. Dis Colon Rectum 2011;54:318–23.
- 39
- Myer ENB, Petrikovets A, Slocum PD ym. Risk factors for explantation due to infection after sacral neuromodulation: a multicenter retrospective case-control study. Am J Obstet Gynecol 2018;219:78.e1-78.e9. doi: 10.1016/j.ajog.2018.04.005
- 40
- Altomare DF, Giuratrabocchetta S, Knowles CH ym. Long-term outcomes of sacral nerve stimulation for faecal incontinence. Br J Surg 2015;102:407–15.
Sacral neuromodulation treatment for fecal incontinence
Sacral neuromodulation has become the primary treatment option for fecal incontinence refractory to conservative treatment. It is estimated that around 5% of the Finnish adult population suffer from fecal incontinence. Though the symptoms of fecal incontinence vary from gas incontinence to inability to contain solid stools, it has a dramatic negative effect on the quality of life.
Most patients with fecal incontinence can be treated conservatively with fibre supplementation, anti-diarrhoeal agents and bowel irrigation. Patients who have failed to improve with the best available conservative treatment could be considered for sacral neuromodulation treatment. Sacral neuromodulation was developed in 1982, the first devices were implanted in Finland in 1996 for urinary incontinence. The first device for fecal incontinence was implanted in 1999 in Oulu University Hospital. In Finland about 90 patients are treated with sacral neuromodulation annually.
The complications of sacral neuromodulation are usually mild infections or pain at the operation site that can be treated conservatively. More serious complications requiring device explantation occur rarely.
Finnish long-term results of sacral neuromodulation treatment for fecal incontinence are yet to be published. Large European multicentre studies have indicated a more than 80% success rate for patients with fecal incontinence in the long term.