Yhdistelmähoito yleisin tuoreeseen nivelreumaan – tulokset hyviä
Lähtökohdat Arvioimme varhaisen nivelreuman hoitolinjoja ja -tuloksia Suomessa.
Menetelmät Selvitimme Taysissa 2012–2019 (n = 359) sekä Suomessa 2016–2021 (Reumarekisteri, n = 6 705) nivelreumadiagnoosin saaneiden ensimmäisen reumalääkityksen, sairauden aktiivisuuden ja biologisen hoidon aloituksen ensimmäisenä vuonna. Analysoimme riittämätöntä vastetta ennustavia tekijöitä.
Tulokset Tays-potilaista 84,7 % aloitti yhdistelmähoidon. Nivelreuman aktiivisuus väheni huomattavasti kolmen kuukauden aikana, ja vuoden kuluttua aloituksesta remissiossa oli 66,7 % potilaista. Aktiivinen tauti, korkea ikä, heikentynyt toimintakyky ja hoidon aloitus monoterapialla ennustivat riittämätöntä vastetta. Reumarekisterin potilaista yhdistelmähoidon aloitti 65 %. Vuoden kuluttua remissiossa oli noin 70 % monitoroiduista potilaista. Biologisen hoidon aloitti molemmissa kohorteissa alle 10 % potilaista.
Päätelmät Yhdistelmähoitoa käytetään varhaiseen nivelreumaan usein, ja noin kaksi kolmasosaa saavuttaa aikaisen remission. Biologisen lääkityksen käyttö hoidon alkuvaiheessa on vähäistä. Erityisen aktiivista tautia sairastavat tai huonosti perinteisille lääkkeille vastaavat potilaat olisi hyvä tunnistaa. Tämä voisi mahdollistaa biologisen tai synteettisen täsmälääkityksen käytön varhain.
Nivelreuma ilmenee nivelten turvotuksena, arkuutena ja aamujäykkyytenä ja on yksi yleisimmistä pitkäaikaisista tulehduksellisista sairauksista (1). Suomessa siihen sairastuu vuosittain noin 1 900 henkilöä (2).
Niveltulehdukset ja -vauriot ovat yhteydessä heikentyneeseen toimintakykyyn ja elämänlaatuun (3,4). Puutteellisesti hoidettuna ne yhdistyvät työkyvyttömyyteen ja ennenaikaiseen eläköitymiseen (5,6).
Tuoreen nivelreuman lääkehoidon tavoitteena on remissio (7,8,9,10). Perustana ovat perinteiset antireumaatit, erityisesti metotreksaatti yksin tai yhdistettynä muihin lääkkeisiin (7). Suomessa varhaiseen aktiiviseen nivelreumaan suositellaan aloittamaan yhdistelmähoito (REKO-hoito), johon kuuluvat metotreksaatti, sulfasalatsiini, hydroksiklorokiini ja pieniannoksinen glukokortikoidi (2,11). Mikäli haluttua vastetta ei saavuteta perinteisillä antireumaateilla, tulee aloittaa biologinen tai pienimolekylaarinen täsmälääkitys (7).
Suomessa on jo vuodesta 1999 alkaen kerätty rekisteritietoa reumapotilaiden hoitotuloksista. Keruussa on ensin keskitytty biologisia lääkkeitä käyttäviin potilaisiin (ROB-FIN-tutkimus). Myöhemmin rekisteri on laajentunut kaikkiin reumapotilaisiin.
Vuoden 2023 alusta Tulehduksellisten reumatautien laaturekisteri (Reumarekisteri) on ollut THL:n ylläpitämä lakisääteinen rekisteri. Tavoitteena on tuottaa järjestelmällistä ja yhdenmukaista tietoa reumasairauksien hoidosta ja hoitotuloksista eri puolilla maata. Rekisterin avulla on analysoitu eri sairauksien hoitotuloksia vuoden kuluttua sairastumisesta. Potilaiden monitorointikattavuus on tosin vaihdellut alueittain, mikä on vaikeuttanut tulosten vertailua.
Kartoittaaksemme Suomessa varhaiseen nivelreumaan käytettyä hoitolinjaa ja -tuloksia tarkastelimme ensin yksityiskohtaisesti vuosina 2012–2019 Taysissa nivelreumadiagnoosin saaneita potilaita. Vertailuna käytimme vuosina 2016–2021 nivelreumadiagnoosin saaneita potilaita Reumarekisteristä.
Aineisto ja menetelmät
Tays-kohortti
Tutkimukseen kerättiin Taysissa aikavälillä 1.1.2012–17.3.2019 nivelreumadiagnoosin saaneet. Potilaita seurattiin noin vuoden ajan ja hoitovaste arvioitiin 3:n (60–150 vrk), 6:n (151–270 vrk) ja 12 kuukauden (271–450 vrk) ajankohdissa. Yksilöllisistä syistä toteutuneet aikahaarukat olivat varsin laajat.
Niveltulehduksen aktiivisuuden mittaamisessa ja remission määrittelyssä käytettiin 28 nivelen mukaan laskettua tautiaktiivisuusindeksiä DAS28 (disease activity score 28). Indeksi huomioi turvonneiden ja arkojen nivelten määrän sekä laskon. Potilailta tuli löytyä tieto DAS28-arvosta GoTreatIt-monitorointiohjelmasta sekä diagnoosivaiheesta että vähintään yhdeltä seurantakäynniltä. Tämän vuoksi kohortista on jouduttu rajaamaan pois 29 % potilaista.
Monitorointiohjelmasta kerättiin tiedot potilaiden painoindeksistä, seropositiivisuudesta, DAS28-arvosta, laskosta, CRP:stä, turvonneiden ja arkojen nivelten lukumääristä, kivusta, yleisvoinnista, väsymyksestä, aamujäykkyydestä, toimintakyvystä, tupakoinnista, koulutusvuosista, työmarkkinastatuksesta, asumismuodosta ja liikunnan määrästä. Remission rajaksi määritettiin DAS28-arvo alle 2,6.
Lisäksi analysoitiin potilaille diagnoosivaiheessa aloitettu lääkitys. Lääkemuutoksia ei huomioitu, lukuun ottamatta biologisen lääkkeen tai januskinaasin (JAK) estäjän aloitusta sekä glukokortikoidin käyttöä 12 kuukauden kohdalla. Potilaat jaettiin aloitetun lääkityksen perusteella neljään ryhmään, joiden DAS28-remission saavuttamista vertailtiin keskenään.
Perinteisten antireumaattien teho katsottiin riittämättömäksi, mikäli vähintään yksi seuraavista seikoista toteutui: 12 kuukauden seurannassa potilas ei saavuttanut remissiota, jouduttiin aloittamaan biologinen lääke, tai potilas käytti glukokortikoidia vuoden kuluttua seurannan aloituksesta.
Reumarekisteri
THL:n Reumarekisterin tiedot kerätään Kelan etuustiedoista (lääkekorvausoikeudet ja sairausvakuutuskorvattavat lääketoimitukset), Kanta Reseptikeskuksesta (lääkemääräykset ja -toimitukset) ja hyvinvointialueiden erikoissairaanhoidon tietojärjestelmien monitorointiohjelmista (potilaiden sairauden aktiivisuuden yksityiskohtainen arviointi).
Poimimme kaikki 2016–2022 nivelreumaan erityiskorvattavuuden saaneet potilaat. Analysoimme heille ensimmäiseksi aloitetun reumalääkityksen sekä vuoden sisään aloitetun biologisen hoidon tai JAK-estäjän. Lisäksi analysoimme 2016–2021 sairastuneiden potilaiden DAS28-arvon lääkityksen aloitushetkellä ja vuoden kuluttua diagnoosista.
Tilastolliset analyysit
Luokittelevat muuttujat kuvaillaan frekvenssijakaumin ja jatkuvat mediaanein ja kvartiilein. Vertailtavien ryhmien erojen testauksessa käytettiin luokittelevissa muuttujissa ristiintaulukointia ja khiin neliö -testiä sekä jatkuvissa muuttujissa Mann-Whitneyn U-testiä. Tilastollisen merkitsevyyden rajana pidettiin p-arvoa < 0,05.
Tulokset
Tays-kohortti
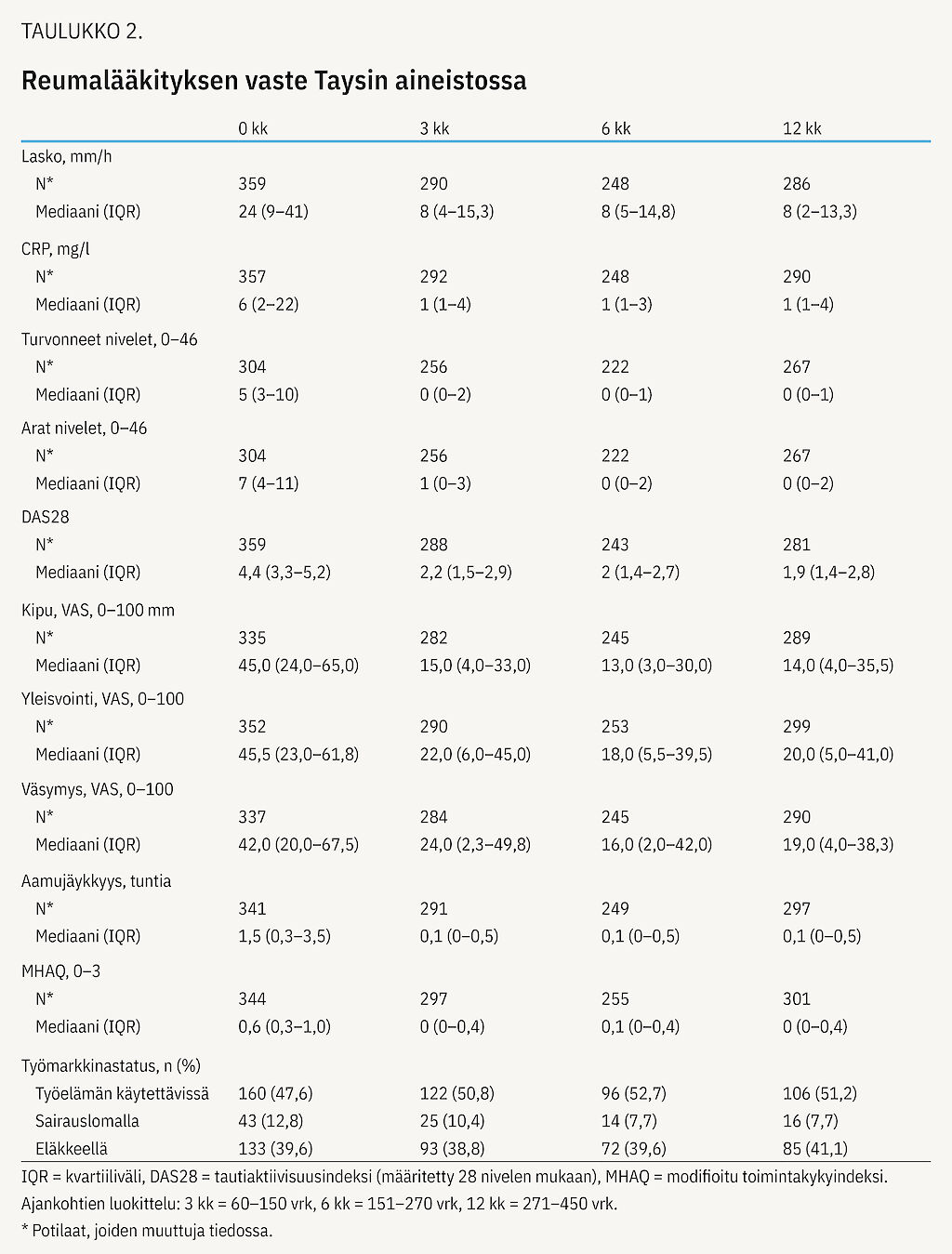
Tays-kohorttiin kuului 359 potilasta, joista naisia oli 70,5 % ja seropositiivisia 73,8 %. Diagnoosivaiheessa potilaiden iän mediaani oli 58,6 vuotta (kvartiiliväli 44,2–67,9) ja DAS28-arvon 4,4 (kvartiiliväli 3,3–5,2). Muut diagnoosivaihetta kuvaavat tiedot on esitetty taulukossa 1.
Potilaista 26,5 %:lle aloitettiin REKO-yhdistelmähoito. Jokin muu metotreksaatin sisältävä perinteisten antireumaattien yhdistelmähoito aloitettiin 49,9 %:lle ja 8,3 %:lle yhdistelmähoito, joka ei sisällä metotreksaattia. 15,3 %:lle lääkehoito aloitettiin monoterapiana, joko jollakin perinteisellä antireumaatilla (glukokortikoidin kanssa tai ilman) tai pelkällä glukokortikoidilla. Metotreksaatti yhdistettynä glukokortikoidiin aloitettiin 5,0 %:lle ja metotreksaatti sellaisenaan 2,5 %:lle.
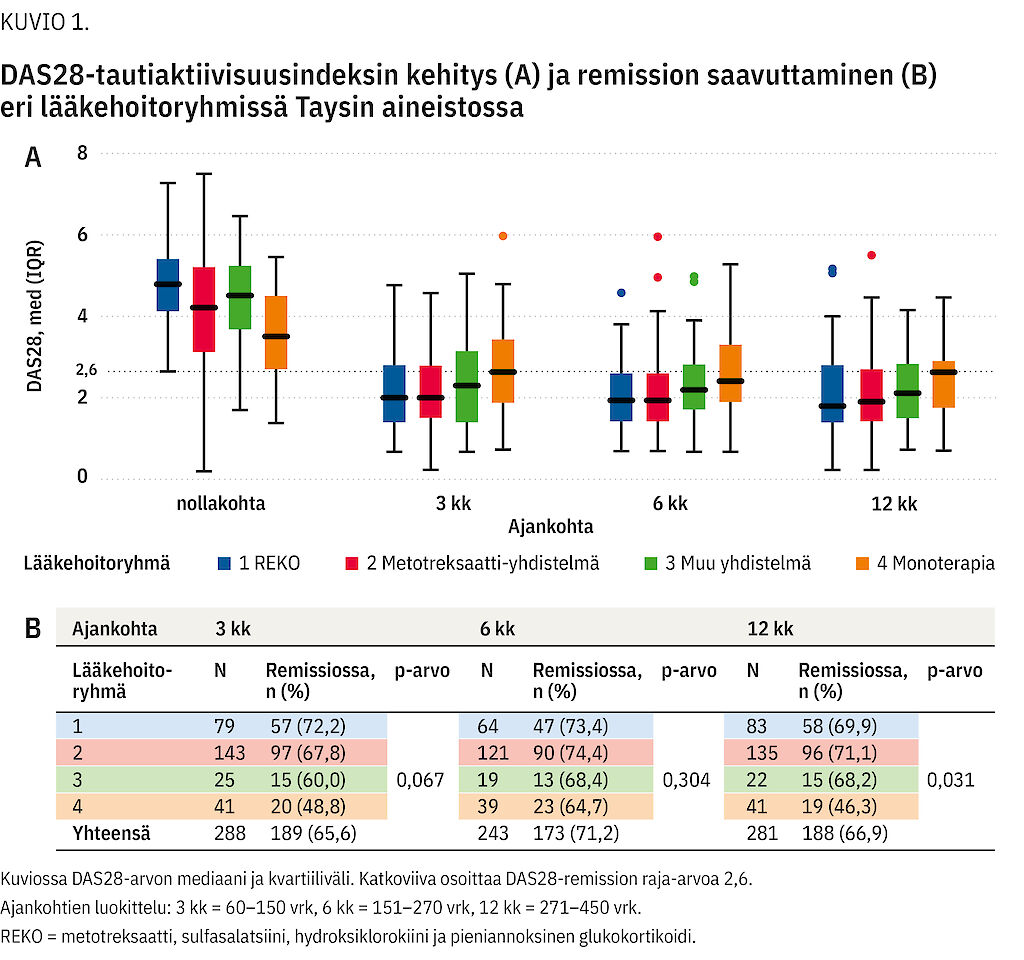
Lääkityksen aikana potilaiden vointi parani ja taudin aktiivisuus väheni merkittävästi vuoden seurannassa (taulukko 2). Suurin parannus nähtiin kolmen kuukauden kohdalla, minkä jälkeen oireet ja nivelreuman aktiivisuus pysyivät stabiilina. DAS28-remissiossa oli 3:n, 6:n ja 12 kuukauden kohdalla 65,6, 71,2 ja 66,7 % potilaista.
Potilaat, joiden hoito aloitettiin monoterapialla, saavuttivat remission harvemmin (vuoden kuluttua 46,3 % remissiossa) kuin potilaat, joiden hoito aloitettiin yhdistelmälääkityksellä (70,4 % remissiossa). Diagnoosivaiheessa sairauden aktiivisuus oli kuitenkin monoterapiaryhmässä pienintä (kuvio 1). Ero vasteessa oli tilastollisesti merkitsevä 12 kuukauden kohdalla (p = 0,031). Eri yhdistelmälääkeryhmissä remission saavuttaneiden potilaiden osuus oli sama.
Valtaosaa potilaista hoidettiin perinteisillä reumalääkkeillä ensimmäisen vuoden aikana. 4,5 %:lle aloitettiin jokin biologinen lääke. Glukokortikoidi oli vuoden kohdalla käytössä 30,4 %:lla. Glukokortikoidia käyttävistä noin puolet oli remissiossa, osalta tieto puuttui.
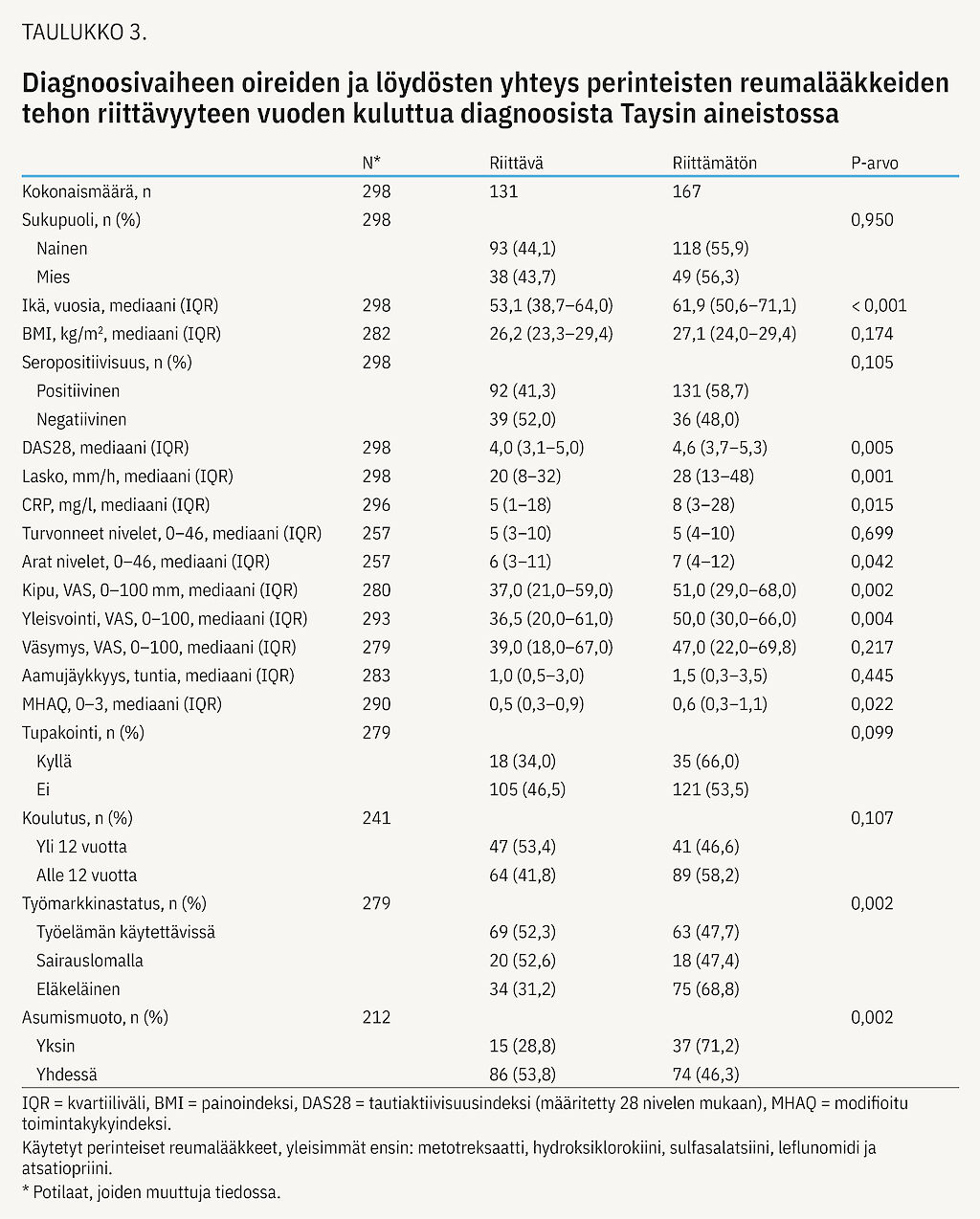
Menetelmät-osiossa kuvatuilla kriteereillä 167 potilaalla perinteisten lääkkeiden teho osoittautui riittämättömäksi. 131:llä teho oli riittävä. 61:ltä tieto puuttui.
Diagnoosivaiheen muuttujien yhteyttä perinteisten reumalääkkeiden tehon riittävyyteen on kuvattu taulukossa 3. Lähtövaiheen muuttujista ikä, DAS28-arvo, lasko, CRP, arkojen nivelten lukumäärä, kipujana (VAS, visual analogue scale), yleisvointi-VAS sekä MHAQ (modified health assessment questionnaire) -indeksi olivat tilastollisesti merkitsevästi yhteydessä lääkityksen tehoon: mitä suurempi luku, sitä riittämättömämpi oli teho. Lisäksi eläkkeellä olevilla ja yksin asuvilla hoidon teho oli merkitsevästi huonompi kuin verrokkiryhmillä.
Reumarekisteri
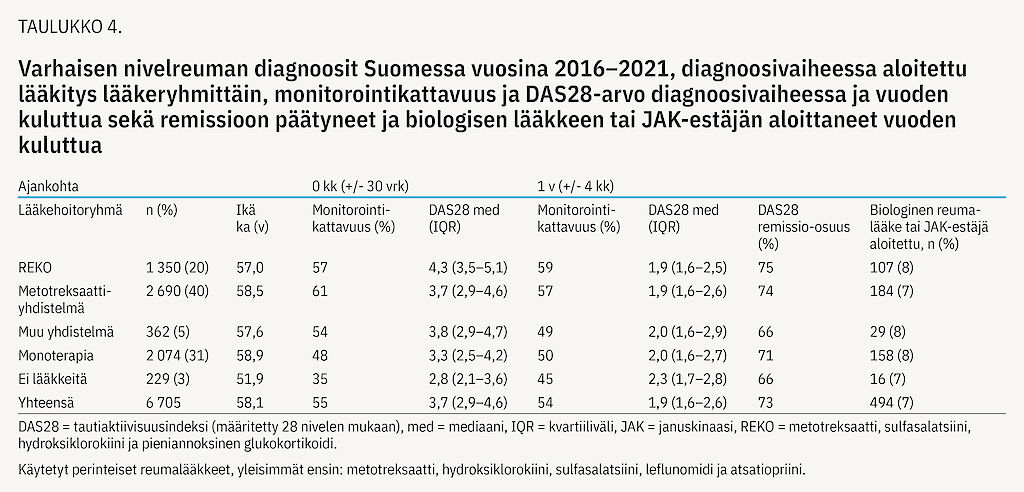
Reumarekisterin potilaat 2016–2021 jaoteltiin aloitetun lääkityksen mukaan vastaaviin ryhmiin kuin Taysin potilaat. Monoterapia (31 % potilaista) oli yleisempää kuin Taysin kohortissa, vaikka jokin yhdistelmä olikin käytössä 65 %:lla (taulukko 4). REKO-hoito aloitettiin 19 %:lle potilaista. Metotreksaatti yhdistettynä glukokortikoidiin aloitettiin 14 %:lle ja metotreksaatti sellaisenaan 12 %:lle.
Biologinen hoito tai JAK-estäjä aloitettiin vuoden aikana 7–8 %:lle riippumatta aloituslääkityksestä.
Sairauden aktiivisuuden arviointia sekä diagnoosivaiheessa että vuoden kohdalla rajoitti monitorointikattavuus. Se vaihteli 35:stä 61 %:iin ajankohdan ja lääkehoitoryhmän mukaan. Kattavimmin monitoroituja olivat potilaat, joille oli aloitettu yhdistelmähoito. Eri hoidoilla saavutetuista tuloksista ei voitu tehdä tilastoanalyyseja, mutta monitoroiduista potilaista 66–75 % oli DAS28-remissiossa vuoden kohdalla (taulukko 4).
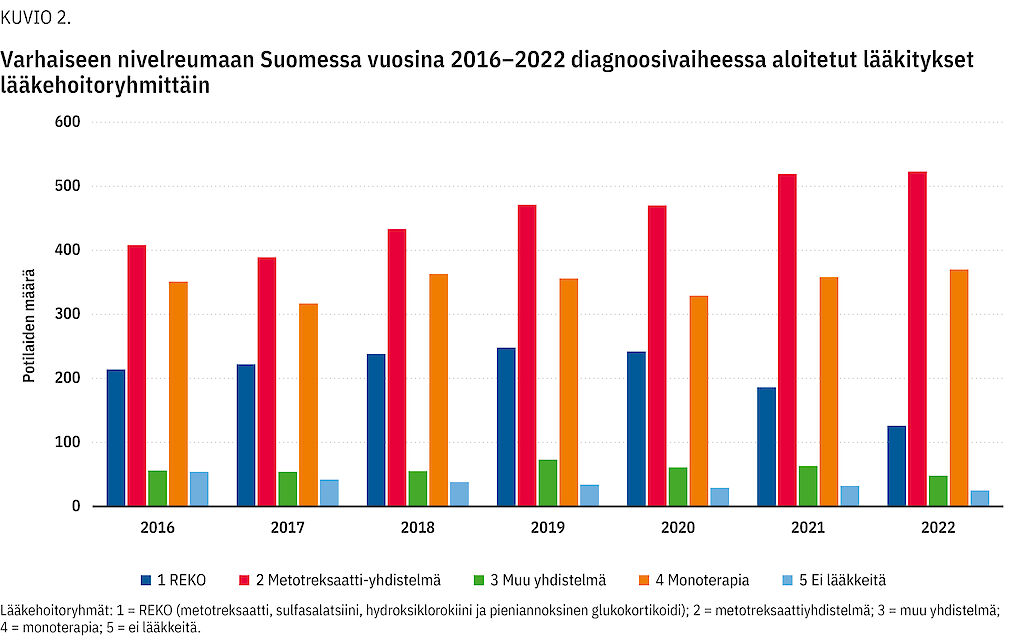
Vuosikohorteittain 2016–2022 analysoituna voitiin todeta, että metotreksaattiyhdistelmän käyttö yleistyi jatkuvasti. Vuoden 2020 jälkeen REKO-hoidon käyttö väheni (kuvio 2).
Päätelmät
Valtaosaa Taysin potilaista hoidettiin perinteisillä lääkkeillä ensimmäisen vuoden aikana. Vaste oli keskimäärin hyvä: suurin osa potilaista päätyi remissioon ja vointi parani kaikilla mittareilla.
Samansuuntaisia hyviä hoitotuloksia on aiemmin raportoitu suomalaisessa tuoreen nivelreuman seurantatutkimuksessa (12). Noin kaksi kolmasosaa potilaista saavutti remission kolmen kuukauden seurannassa. Tätä voi pitää hyvänä vasteena, sillä lääkityksen tavoitteena on remission saavuttaminen kolmen tai viimeistään kuuden kuukauden aikana (7). Remissiossa olevien potilaiden osuus pysyi tasaisena kolmen kuukauden jälkeen vuoden seurannassa. Reumarekisterin tulosten perusteella remissiossa olevien osuus pitkään kestäneessä nivelreumassa on vastaavaa luokkaa (13).
Monoterapialla aloittaneella potilasryhmällä taudin keskimääräinen aktiivisuus oli lähtövaiheessa vähäisin. Tästä huolimatta ryhmä päätyi huonoimpaan hoitotulokseen. Tämä on linjassa aiempien tutkimustulosten kanssa (11). Lisäksi se tukee ajatusta, että alkuhoidon tulee olla riittävän tehokasta myös lievemmässä nivelreumassa.
Sen sijaan REKO-hoidon ja muiden yhdistelmälääkitysten tehoissa ei ollut eroa. Tämä osoittaa, että REKO-hoitoa kevyemmälläkin yhdistelmähoidolla voidaan päästä hyvään hoitotulokseen.
Tiukasti arvioituna perinteisten reumalääkkeiden teho ei riittänyt merkittävälle osalle potilaista, koska kolmannes ei saavuttanut remissiota ja noin kolmannes oli joutunut käyttämään glukokortikoidia vielä vuoden kohdalla. Glukokortikoidin lyhytaikaisen käytön on perinteisiin antireumaatteihin yhdistettynä havaittu lieventävän taudin aktiivisutta (14,15). Pitkäaikaiseen käyttöön liittyy kuitenkin useita haittavaikutuksia (16).
Riittämätöntä vastetta ennusti taudin suurempi aktiivisuus lähtötilanteessa. Lisäksi reumalääkkeiden teho oli heikompi iäkkäillä, eläkeläisillä ja yksin asuvilla. Iäkkäillä hoitostrategiaan saattaa vaikuttaa liitännäissairauksien esiintyvyys. Tässäkin potilasryhmässä tulisi silti pyrkiä mahdollisimman tehokkaaseen lääkehoitoon.
Reumarekisterin tulokset osoittavat, että metotreksaattiyhdistelmä on Suomessa varhaisessa nivelreumassa käytetyin hoitostrategia. Monoterapia aloitetaan kolmasosalle potilaista. Monoterapialla aloittavista alle puolet on monitoroitu sairauden alkuvaiheessa. Tämä saattaa olla merkki muutoinkin passiivisemmasta hoitokulttuurista.
Toisaalta biologisen hoidon tai JAK-estäjän aloitukseen päätyy sama osuus potilaista riippumatta aloituslääkityksestä. Se onkin ainut kattavasti arvioitavissa oleva päätetapahtuma Reumarekisteri-kohortissa. Prosenttiosuus on myös vähän suurempi kuin aktiivisesti hoidetuilla Taysin potilailla.
Tämän tutkimuksen tulokset tarjoavat näytteen siitä, miten yksityiskohtaisesti reumapotilaiden hoidon vaikuttavuutta voi analysoida. Kaikkien hyvinvointialueiden tulisi sisäistää Reumarekisterin lakisääteisyys osaksi toimintaansa ja panostaa monitoroinnin kattavuuteen. Tällöin analysointia voitaisiin tehdä valtakunnallisesti.
Biologinen lääkitys aloitettiin vuoden seurannassa vain harvalle, mikä on linjassa aiempien tulosten kanssa (2). Toisaalta noin kolmannes potilaista ei saavuttanut remissiota seurannassa. Biologinen lääkitys on käytössä noin 20 %:lla yli kaksi vuotta nivelreumaa sairastaneista (17). Biologisten lääkkeiden aktiivisemmasta käytöstä saattaisikin olla hyötyä myös varhaisessa nivelreumassa.
Pohjoismaisessa tutkijalähtöisessä tutkimuksessa aloitettiin heti joko optimoitu perinteinen lääkehoito tai vaihtoehtoisesti metotreksaatti yhdistettynä biologiseen lääkkeeseen (18). Vuoden kohdalla hoito T-soluestäjä abataseptilla tai TNF-salpaaja sertolitsumabilla osoittautui tehokkaammaksi (DAS28-remissiossa 71,1 tai 66,6 %) kuin perinteinen hoito (remissiossa 53,7 %). Tutkimus korostaa, että varhainen biologinen lääkitys on tehokas aktiivisessa nivelreumassa.
Hoito biologisin reumalääkkein on kalliimpaa kuin perinteisin lääkkein. Toisaalta myös teholtaan riittämätön hoito aiheuttaa huomattavia kustannuksia (7). Edullisempien biosimilaarien ja rinnakkaislääkkeiden yleistyessä biologisten lääkkeiden käyttö sairauden varhaisvaiheessa voi olla myös farmakoekonomisesti kannattavaa.
Tämän tutkimuksen vahvuus on valikoitumaton potilasaineisto, joka kuvastaa nivelreuman hoitoa tosielämässä. Toisaalta osa tiedoista oli puutteellisia, minkä vuoksi kaikkia päätetapahtumia ei pystytty analysoimaan yhtä luotettavasti kuin kontrolloiduissa lääketutkimuksissa. Tämä tuli esiin myös Reumarekisterin aineistossa, jossa puutteellinen monitorointikattavuus esti hyvin yksityiskohtaiset analyysit.
Yhteenvetona voidaan todeta, että varhaisen nivelreuman hoito toteutetaan pääosin perinteisten reumalääkkeiden yhdistelmillä. Hoitotulokset ovat kansainvälisestikin arvioiden hyviä. Biologisten ja pienmolekylaaristen täsmälääkkeiden aloitus tulisi kohdistaa potilaisiin, joilla perinteisten reumalääkkeiden teho jää riittämättömäksi. Toisena kohderyhmänä voisivat jatkossa olla ehkä myös potilaat, joilla alun alkaen on aggressiivinen tauti.
Kiitämme Taysin Kliininen informatiikka -tiimin jäseniä Sampo Kukkuraista ja Toni Mikkolaa Taysin datan keräämisestä ja käsittelystä ja laatusihteeri Tuula Reiniä datan tarkistamisesta sekä Taysin tutkimusjohtajaa Tarja Laitista avusta projektin käynnistämisessä ja edistämisessä. Kiitämme Reumarekisterin ydinryhmän jäseniä Johanna Kärkeä, Laura Kuusaloa, Tuulikki Sokka-Isleriä, Paula Vähäsaloa, Maria Bäcklundia, Johanna Huhtakangasta, Tero Pääkköä, Heikki Relasta, Jarno Rutasta ja Anniina Pylsyä Reumarekisterin aineiston ja THL:n statistikko Henri Salon työpanoksen myöntämisestä tutkimusryhmän käyttöön. Vappu Rantalaiho kuuluu Reumarekisterin ydinryhmään.
Iida Kauppi, Veli Valkokari, Paula Muilu, Mika Helminen, Henri Salo: Ei sidonnaisuuksia.
Dan Nordström: Konsultointi (BMS, MSD, Novartis, Pfizer, UCB), apuraha (MSD), korvaus koulutusaineiston tuottamisesta (Duodecim).
Vappu Rantalaiho: Apurahat (Pirkanmaan Hyvinvointialue, Kanta-Hämeen Hyvinvointialue, Wilhelm och Else Stockmanns stiftelse), luentopalkkiot (Novartis, Viatris, Abbvie), korvaus koulutusaineiston tuottamisesta (Duodecim).
Pia Isomäki: Apurahat (Tays tukisäätiö, Valtion tutkimusrahoitus), konsultointi (Eli Lilly, Fresenius Kabi, Galapagos, ViforPharma), luentopalkkiot (Galapagos, Pfizer, Novartis, Labquality Days, Tampereen ammattikorkeakoulu), korvaus koulutusaineiston tuottamisesta (Farmasian oppimiskeskus).
Tämä tiedettiin
• Suomalaisissa kliinisissä tutkimuksissa tuoreen nivelreuman hoitotulokset ovat olleet erinomaiset, mutta vähemmän on tietoa hoitotuloksista tosielämän potilailla.
• Käypä hoito suosittaa varhaisen nivelreuman hoidoksi REKO-yhdistelmähoitoa. Sen ja muiden perinteisten reumalääkkeiden yhdistelmähoitojen käytöstä tosielämän potilailla ei kuitenkaan ole tutkittua tietoa.
Tutkimus opetti
• Tosielämän nivelreumapotilaista noin kaksi kolmasosaa on remissiossa vuoden kuluttua diagnoosista. Tätä voidaan pitää hyvänä hoitotuloksena.
• Varhaisen nivelreuman hoidossa käytetään ensisijaisesti perinteisten reumalääkkeiden yhdistelmähoitoja. Biologisten lääkkeiden käyttö on vähäistä. Monoterapia ei ole yhtä tehokas kuin yhdistelmälääkitys.
• Riittävän tehokkaaseen hoidon aloitukseen kannattaa kiinnittää huomiota erityisesti iäkkäillä sekä heillä, joiden sairaus alkaa tavanomaista aktiivisempana.
- 1
- Di Matteo A, Bathon JM, Emery P. Rheumatoid arthritis. Lancet 2023;402:2019–33.
- 2
- Muilu P, Rantalaiho V, Kautiainen H, Virta LJ, Eriksson JG, Puolakka K. First-year drug therapy of new-onset rheumatoid and undifferentiated arthritis: a nationwide register-based study. BMC Rheumatol 2020;4:34.
- 3
- Welsing PMJ, Van Gestel AM, Swinkels HL, Kiemeney LALM, Van Riel PLCM. The relationship between disease activity, joint destruction, and functional capacity over the course of rheumatoid arthritis. Arthritis Rheumatol 2001;44:2009–17.
- 4
- Nikiphorou E, Norton SJ, Carpenter L ym. Remission vs low disease activity: function, quality of life and structural outcomes in the Early Rheumatoid Arthritis Study and Network. Rheumatology (Oxford) 2020;59:1272–80.
- 5
- Puolakka K, Kautiainen H, Rantalaiho V, Virta L, Sokka-Isler T, Haanpää M. Reumapotilaiden siirtyminen työkyvyttömyyseläkkeelle vaihtelee sairaanhoitopiireittäin. Suom Lääkäril 2019;74:754–60.
- 6
- Kerola A, Kauppi M, Nieminen T ym. Psychiatric and cardiovascular comorbidities as causes of long-term work disability among individuals with recent-onset rheumatoid arthritis. Scand J Rheumatol 2015;44:87–92.
- 7
- Smolen JS, Landewé RBM, Bergstra SA ym. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2022 update. Ann Rheum Dis 2023;82:3–18.
- 8
- Sokka T. T2T-manifesti tähtää nivelreuman parempaan hoitoon. Suom Lääkäril 2011;66:1472–3.
- 9
- Smolen JS, Aletaha D, Bijlsma JWJ ym. Treating rheumatoid arthritis to target: recommendations of an international task force. Ann Rheum Dis 2010;69:631–7.
- 10
- Suomalaisen Lääkäriseuran Duodecimin ja Suomen Reumatologisen yhdistyksen asettama työryhmä. Nivelreuma. Käypä hoito -suositus 8.9.2022. www.kaypahoito.fi
- 11
- Rantalaiho V, Puolakka K, Korpela M, Hannonen P, Möttönen T. Long-term results of the FIN-RACo trial; treatment with a combination of traditional disease-modifying anti-rheumatic drugs is an excellent option in early rheumatoid arthritis. Clin Exp Rheumatol 2012;30:S27–31.
- 12
- T Rannio, J Asikainen, P Hannonen, ym. Three out of four disease-modifying anti-rheumatic drug-naïve rheumatoid arthritis patients meet 28-joint Disease Activity Score remission at 12 months: results from the FIN-ERA cohort. Scand J Rheumatol 2017;46:425–31.
- 13
- Weman L, Salo H, Kuusalo L ym. Similar levels of disease activity and remission rates in patients with psoriatic arthritis and rheumatoid arthritis-results from the Finnish quality register. Clin Rheumatol 2024;43:633–43.
- 14
- Boers M, Hartman L, Opris-Belinski D ym. Low dose, add-on prednisolone in patients with rheumatoid arthritis aged 65+: the pragmatic randomised, double-blind placebo-controlled GLORIA trial. Ann Rheum Dis 2022;81:925–36.
- 15
- Hua L, Du H, Ying M ym. Efficacy and safety of low-dose glucocorticoids combined with methotrexate and hydroxychloroquine in the treatment of early rheumatoid arthritis: a single-center, randomized, double-blind clinical trial. Medicine 2020;99:e20824.
- 16
- Da Silva JAP. Safety of low dose glucocorticoid treatment in rheumatoid arthritis: published evidence and prospective trial data. Ann Rheum Dis 2006;65:285–93.
- 17
- Kärki J, Rantalaiho V, Kuusalo L ym. Vuosiraportti 2023. Tulehduksellisten reumasairauksien laaturekisteri, Reumarekisteri 2023. https://www.reumatologinenyhdistys.fi/vuosiraportit/
- 18
- Østergaard M, van Vollenhoven RF, Rudin A ym. Certolizumab pegol, abatacept, tocilizumab or active conventional treatment in early rheumatoid arthritis: 48 week clinical and radiographic results of the investigator-initiated randomized controlled NORD-STAR trial. Ann Rheum Dis 2023;82:820–8.
Combination therapy most common for early rheumatoid arthritis – results are good
Background We evaluated current treatment choices and results in early rheumatoid arthritis (RA) in Finland.
Methods Initial medication, disease activity and initiation of biologic therapy within one year were analysed in 359 RA patients from Tampere University Hospital (Tays) diagnosed between 2012-2019 and in 6705 patients from the FinRheuma Register diagnosed between 2016-2021. Factors predicting inadequate response to therapy were also evaluated.
Results Combination therapy was started by 84,7% of Tays patients. RA disease activity diminished significantly within 3 months. At 12 months 66,7% were in remission. High disease activity, older age, loss of function and monotherapy were factors predicting inadequate treatment response. FinRheuma Register patients were treated with combination therapy in 65% of cases. At 12 months approximately 70% of monitored patients were in remission. In both cohorts biologic therapy was initiated in <10% of patients.
Conclusions Combination therapy is widely used in patients with early RA leading to remission in two thirds of cases. The use of biologic therapy within one year is sparse. Being able to identify patients with high disease activity or experiencing poor response to conventional therapy gives room for early biological or targeted therapy.