Taustatekijät vaikuttavat ALS-potilaiden saattohoitoon ja kuolinpaikkaan
Lähtökohdat Amyotrofinen lateraaliskleroosi (ALS) on harvinainen liikehermosairaus, johon ei ole parantavaa hoitoa. Keskimääräinen elinaika diagnoosista on noin 2–4 vuotta. Tutkimme, missä potilaiden saattohoito toteutui ja millä taustatekijöillä oli yhteys kuolinpaikkaan.
Menetelmät Selvitimme vuosina 2002–2022 ALS:iin menehtyneiden kuolinpaikkaa, parisuhdestatusta, sukupuolta, ikää, kaksoispaineventilaatiohoidon ja ravitsemusletkun käyttöä sekä sitä, oliko näillä yhteyttä kuolinpaikkaan tutkimusjakson aikana.
Tulokset Vuosina 2002–2022 ALS:iin sairastui 299 potilasta, joista 260 menehtyi. 20 % potilaista menehtyi kotona, 28 % terveyskeskusosastolla, 15 % sairaalassa, 13 % saattohoitoyksikössä ja 21 % palvelutalossa. Kotona menehtyneistä 76 % ja sairaalassa menehtyneistä 69 % oli parisuhteessa, kun taas palvelutalossa menehtyneistä 74 % oli yksin asuvia ja valtaosa naisia.
Päätelmät Suurin osa ALS:iin sairastuneista menehtyi muualla kuin kotona. Parisuhdestatuksella, sukupuolella ja iällä saattoi olla yhteys kuolinpaikkaan. Taustatekijöihin on hyvä kiinnittää huomiota saattohoitoa suunniteltaessa. Löydös on tärkeä varmentaa laajemmalla kansallisella aineistolla.
Amyotrofinen lateraaliskleroosi (ALS) on harvinainen liikehermoja rappeuttava sairaus, jonka ilmaantuvuus aikuisväestössä on noin 2–5 potilasta 100 000:ta aikuista kohden (1,2). Ilmaantuvuudessa on havaittu merkittävää maantieteellistä vaihtelua. On arveltu, että Suomessa esiintyvyys on maailman suurinta (3,4,5).
Arviolta 70 %:lla sairaus alkaa toispuoleisena raajalihasheikkoutena, etenee vähitellen vartalon alueelle ja affisioi lopulta kaikkea tahdonalaista lihaskudosta. Noin kolmasosalla sairaus alkaa nielun alueelta, mikä vaikeuttaa syömistä ja puhumista (6).
Vaikka sairauden etiologia on viime vuosikymmenen aikana merkittävästi tarkentunut, ratkaisevaa edistysaskelta parantavan hoidon saralla ei ole kuitenkaan otettu (2). Valtaosa potilaista menehtyy hengitysvajauksen seurauksena (7,8). Keskimääräinen elinajanodote diagnoosista on noin 2–4 vuotta (6).
Kansainvälisten suositusten mukaan ALS:n hoidon tulisi olla moniammatillista ja keskitettyä. Hengitystukihoidoksi suositellaan kasvonaamarin kautta toteutettavaa kaksoispaineventilaatiota (2PV) ja ravitsemuksen tueksi vatsanpeitteiden läpi asetettavaa ravitsemusletkua (percutaneous endoscopic gastrostomy, PEG) (9,10,11). Potilaan ja läheisten toiveita tulee kuunnella, kun oireenmukaista hoitoa ja saattohoitoa suunnitellaan ja toteutetaan (8,10).
Sosiaali- ja terveysministeriön (STM) asettaman kansallisen tavoitetilan mukaan jokaisella iäkkäällä tulisi olla mahdollisuus asua kotona jopa elämänsä loppuun asti. Tavoitteesta huolimatta arviolta lähes puolet yli 70 vuotta täyttäneistä menehtyy terveyskeskuksessa ja vain 15 % kotona (12).
Tämän taannehtivan tutkimuksen tavoite oli selvittää, missä ALS-potilaan saattohoito lopulta toteutui ja oliko potilaan sukupuolella, parisuhdestatuksella, tukihoitojen (2PV-hoito ja PEG-letku) käytöllä tai iällä yhteyttä kuolinpaikkaan Varsinais-Suomen alueella. Lisäksi halusimme tutkia, oliko käytetyillä tukihoidoilla yhteyttä potilaiden elossa oloon.
Aineisto ja menetelmät
Tutkimusaineisto kerättiin takautuvasti Tyksin Hengitystukiyksikön arvioon vuosina 2002–2022 lähetetyistä ALS-potilaista ja sähköiseen potilastietojärjestelmään tallennetuista potilasasiakirjoista. Asiakirjoista tarkistettiin sairauden ensioireen ilmaantumisajankohta ja luonne (raajojen tai vartalon vai nielun alue), diagnoosin ajankohta, sukupuoli, ikä diagnoosihetkellä, ravitsemusletkun asettamisen ajankohta ja 2PV-hoidon aloitusajankohta, hoitohenkilökunnan tekemät kirjaukset 2PV-hoidon ja PEG-letkun käytön aktiivisuudesta (esim. laitteen rekisteröimät keskimääräiset käyttötunnit vuorokaudessa) saattohoitovaiheessa, parisuhdestatus menehtymishetkellä sekä kuolinpaikka (koti, terveyskeskusosasto, sairaala, palvelutalo vai erityistason saattohoitoyksikkö). Pysyvässä hengityskonehoidossa olevat (n = 6) jätettiin pois tutkimuksesta.
Perussairauden diagnoosi tehtiin Tyksin neurologian poliklinikalla. Diagnoosin asettamisesta vastasi neurologian erikoislääkäri. Diagnoosin asettamisen jälkeen potilas siirtyi kuntoutustyöryhmän seurantaan. Ryhmä koostui neurologista, hengitysvajauksen hoitoon perehtyneestä anestesialääkäristä ja hoitajasta, fysioterapeutista, puheterapeutista, ravitsemusterapeutista, sosiaalityöntekijästä sekä vuodesta 2020 lähtien palliatiivisen hoidon lääkäristä ja sairaanhoitajasta. Potilaat kävivät kuntoutustyöryhmän arviossa säännöllisesti 3–6 kuukauden välein.
Sairauden loppuvaiheen hoidon toteutti perusterveydenhuolto tai sosiaalihuolto yhteistyössä erikoissairaanhoidon kanssa potilaan omassa asuinkunnassa. Osa potilaista menehtyi erikoissairaanhoidossa.
Ensioireen luonne ja ilmaantumisajankohta arvioitiin potilaan kertoman perusteella noin kolmen kuukauden tarkkuudella. Sairauden kokonaiskesto laskettiin sekä ensioireen ilmaantumisajankohdasta että diagnoosin asettamisajankohdasta menehtymiseen.
Tutkimuksella oli Varsinais-Suomen sairaanhoitopiirin myöntämä tutkimuslupa ja eettisen toimikunnan puoltava lausunto.
Kuolinpaikkojen yhteyttä taustatekijöihin tutkittiin Fisherin tarkan testin avulla. Diagnoosi-iän ja kuolinpaikan sekä tukihoidon yhteyttä tutkittiin yksisuuntaisen varianssianalyysin avulla. Kuolinajan yhteyttä taustatekijöihin tutkittiin Wilcoxonin testillä ja kuvattiin Kaplan–Meier-kuvaajan avulla. Alle 0,05:n p-arvoja (kaksisuuntainen) pidettiin merkitsevinä. Tilastolliset analyysit tehtiin SAS-ohjelmistolla (versio 9,4 Windows).
Tulokset
Vuosina 2002–2022 ALS:iin sairastui kaikkiaan 299 potilasta. Heistä 130 (43 %) oli miehiä ja 164 (55 %) parisuhteessa. Menehtyneistä 183:lla (62 %) sairaus alkoi raajojen ja lopuilla nielun alueelta. Potilaiden mediaani-ikä diagnoosihetkellä oli 68 vuotta (vaihteluväli 33–93) ja mediaaniviive ensioireesta diagnoosin asettamiseen 12,5 kuukautta (0–147).
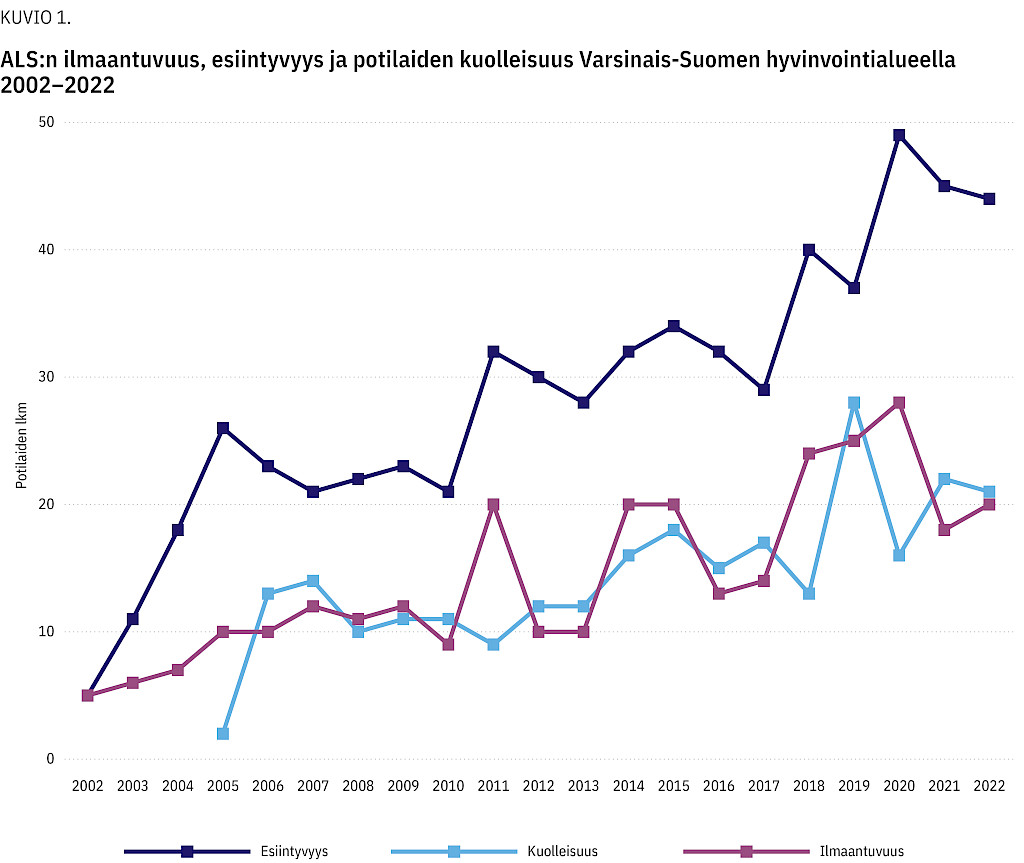
Potilaiden vuosittainen mediaani-ilmaantuvuus oli 12 (5–28), esiintyvyys 29 (5–49) ja kuolleisuus 13 (2–28) potilasta. Seurantajakson aikana ALS-potilaiden mediaani-ilmaantuvuus kasvoi 2,6:sta 4 potilaaseen 100 000 asukasta kohden. Kuviossa 1 on havainnollistettuna potilaiden vuotuinen ilmaantuvuus, kuolleisuus sekä elossa olevien kokonaismäärä seurantajakson aikana.
Tutkimusjakson aikana 260 potilasta (89 % kaikista potilaista) menehtyi. Heistä 52 (20 %) menehtyi kotona, 73 (28 %) terveyskeskuksessa, 40 (15 %) sairaalassa, 54 (21 %) tuetussa palvelutalossa ja 34 (13 %) saattohoitoyksikössä. Taulukossa 1 on esitettynä ALS:iin menehtyneiden lukumäärä jaoteltuna sukupuolen, parisuhdestatuksen, käytössä olleiden tukihoitojen sekä sairastumisiän mukaan eri kuolinpaikoissa.
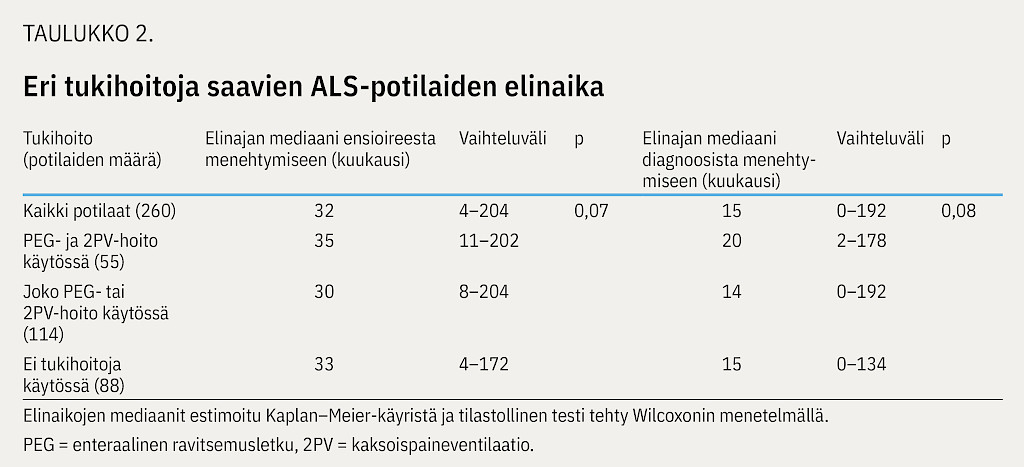
Potilaiden mediaanielinaika ensioireesta menehtymiseen oli 32 kuukautta (4–204). Mediaanielinaika diagnoosista menehtymiseen oli 15 kuukautta (0–192). Heistä 55:llä (21 %) oli menehtyessään käytössä molemmat tukihoidot, 114:llä (44 %) oli vain toinen tukihoito (PEG-letku 74:llä [28 %] ja 2PV-hoito 40:llä [15 %]). Lopuilla 87:llä (33 %) ei ollut kumpaakaan tukihoitoa.
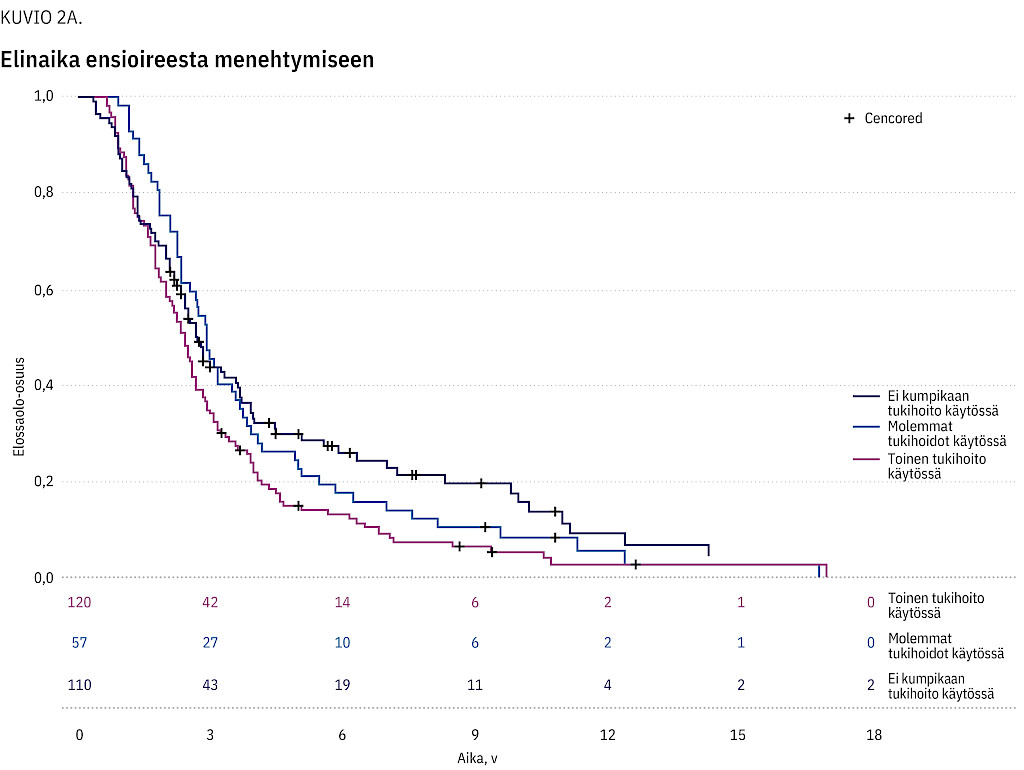
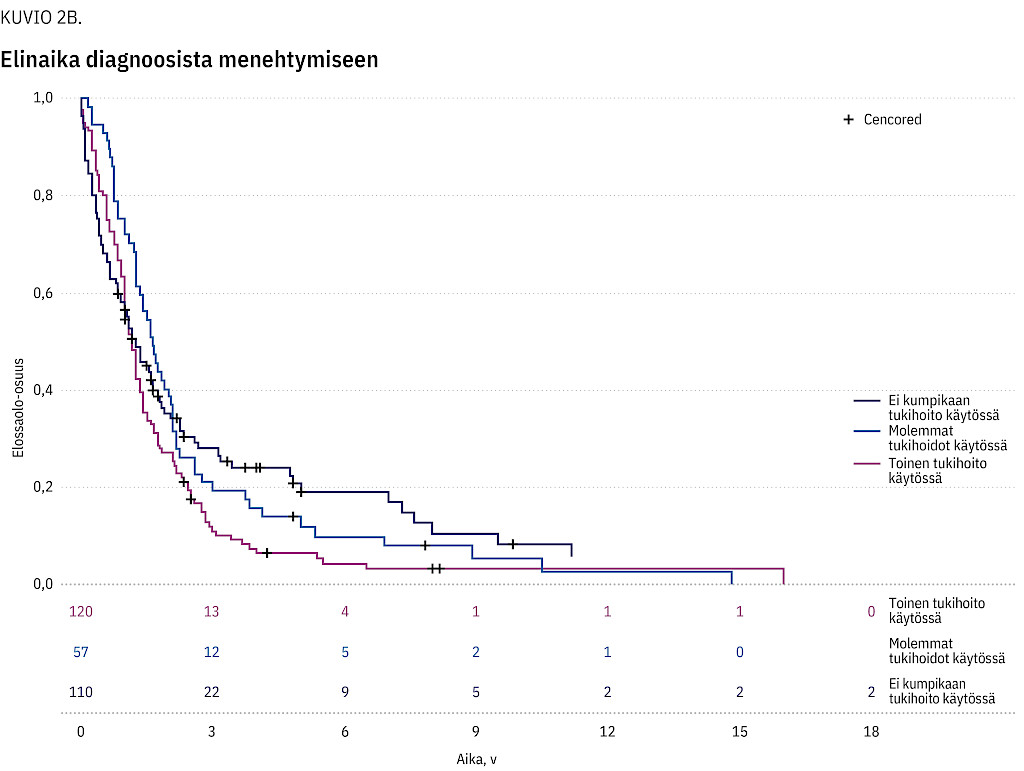
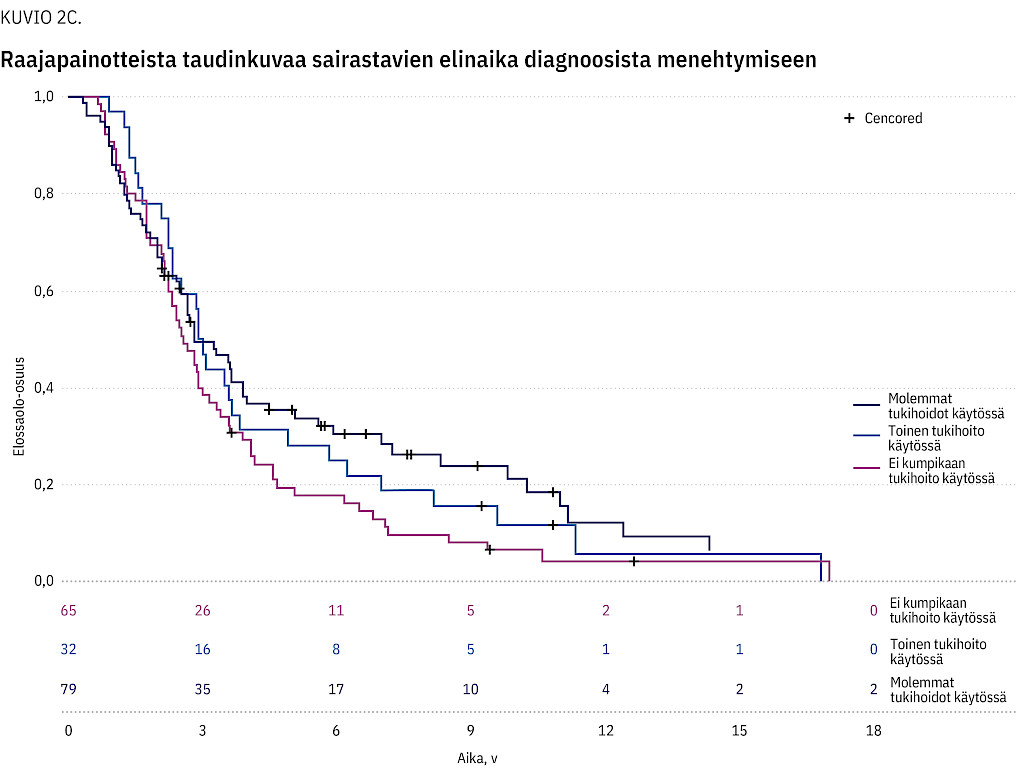
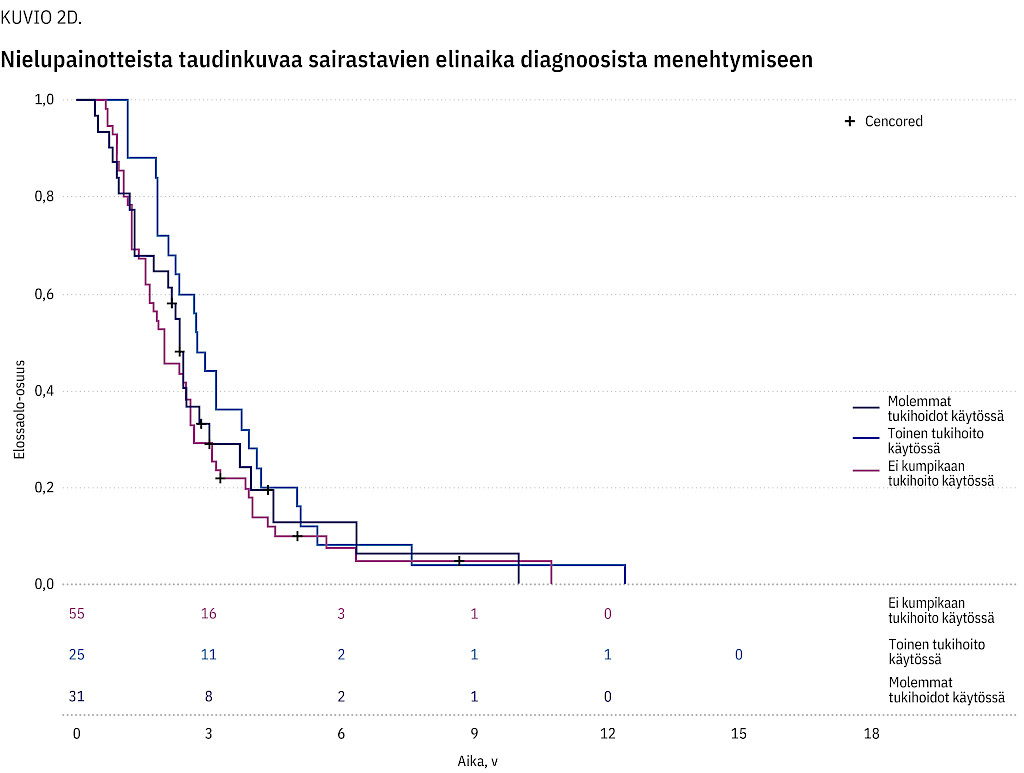
Taulukossa 2 on esitettynä elinajat sekä ensioireen ilmaantumishetkestä että diagnoosista menehtymiseen. Kuviossa 2a on esitettynä potilaiden elinaika ensioireesta menehtymiseen ja kuviossa 2b elinaika diagnoosista menehtymiseen. Kuvioissa 2c ja 2d on esitettynä erikseen raajapainotteista ja nielupainotteista taudinkuvaa sairastavien elinaika diagnoosista menehtymiseen Kaplan–Meier-kuvaajana.
Päätelmät
Kuluneen kahdenkymmen vuoden aikana valtaosa (80 %) ALS:iin sairastuneista menehtyi sosiaali- tai terveydenhuollon yksikössä. Vain joka viides menehtyi kotona.
Löydöksemme on linjassa hiljattain julkaistun ruotsalaistutkimuksen kanssa, jonka mukaan ALS:iin sairastuneista 20 % menehtyi kotona (13). Ruotsalaisten havainnon mukaan kuoleman ennakoitavuudella oli kuitenkin selvä vaikutus siihen, missä potilas kuoli. Jos kuolemaan oli valmistauduttu ennakoivalla hoitosuunnitelmalla, 57 % potilaista menehtyi saattohoitoon perehtyneissä yksiköissä ja vain 7 % sairaalassa. Ennakoivan hoitosuunnitelman puuttuessa jopa 45 % potilaista menehtyi sairaalassa ja vain 28 % saattohoitoyksikössä (13).
Aiemmin syöpäpotilailla tehdyissä tutkimuksissa on havaittu, että potilaat, joilla on hoitosuhde palliatiiviseen yksikköön, menehtyvät harvemmin sairaalassa, kuin potilaat, joilla palliatiivista hoitosuhdetta ei ole (14). STM:n laskelman mukaan tehostettuun palveluasumiseen ja palliatiiviseen hoitoon panostamalla voitaisiin jopa puolittaa niiden potilaiden määrä, jotka hakeutuvat sairaalaan viimeisen kolmen elinkuukautensa aikana (15).
Tulostemme mukaan kotona tai sairaalassa menehtyneille potilaille ominaista oli se, että he olivat keski-iältään nuorempia ja useimmiten parisuhteessa eläviä miehiä. Tuetussa palvelutalossa menehtyneistä taas valtaosa oli keski-iältään vanhempia ja useimmiten yksin asuvia naisia. Oma selityksemme tälle löydökselle perustuu kliiniseen havaintoon: parisuhteessa elävien potilaiden puolisot kokevat herkästi velvollisuudekseen hoitaa sairasta puolisoaan kotona niin pitkään kuin mahdollista. He saattavat jopa kieltäytyä tukeutumasta ulkopuoliseen apuun ja hoitopaikkaan. Yksin asuvat ovat sen sijaan jo olosuhteiden seurauksena pakotettuja ottamaan vastaan ulkopuolista apua.
Mahdollisesti juuri puolison tuen vuoksi saattohoito saattaa parisuhteessa elävillä toteutua useammin kotona. On kuitenkin mahdollista, että kuoleman lähestyessä kynnys hakeutua päivystykselliseen hoitoon saattaa myös heillä madaltua. Tällöin osa heistä menehtyy sairaalassa.
Etenevän raajaheikkouden ja siitä johtuvan toimintakyvyn heikkenemisen voisi ajatella lisäävän ulkopuolisen avun tarvetta erityisesti potilailla, jotka käyttävät sorminäppäryyttä vaativia tukihoitoja, kuten PEG-letkua ja 2PV-hoitoa. Eri kuolinpaikkojen välillä ei kuitenkaan ollut eroa näiden tukihoitojen esiintyvyydessä. Tuloksistamme ei siten voi suoraan tehdä johtopäätöstä, että tukihoitojen käyttäminen heikentäisi mahdollisuutta menehtyä kotona.
Hivenen yllättäen emme kyenneet osoittamaan tilastollisesti merkitsevää yhteyttä tukihoitojen käytön ja elinajan pidentymisen välillä, toisin kuin aiemmissa kansainvälisissä tutkimuksissa on havaittu (16,17,18). Nähdäksemme tukihoitoja ei kuitenkaan pitäisi suosittaa yksinomaan siksi, että ne parantavat elinajanodotetta. Perusteena tulisi käyttää pikemminkin oireita lievittävää ja elämänlaatua parantavaa vaikutusta (8,10).
Seurantajakson aikana ALS:n esiintyvyys Varsinais-Suomen hyvinvointialueella kaksinkertaistui ja oli suurimmillaan jopa 10 potilasta 100 000:ta asukasta kohden (vuosi 2020). Kasvu saattaa selittyä osin diagnostisten menetelmien kehittymisellä, osin myös tilastointiharhalla: aiemmin kaikkia ALS:iin sairastuneita ei lähetetty Hengitystukiyksikön arvioon, joten he jäivät pois ilmaantuvuusanalyysista. Tuloksemme vaikuttaa olevan linjassa Hanhisuannon ym. hiljattain tekemän havainnon kanssa, jonka mukaan sairauden esiintyvyys Varsinais-Suomen alueella oli 11,9 potilasta 100 000:ta asukasta kohden (5).
Tutkimuksemme keskeisin rajoite on takautuva toteuttaminen. On mahdollista, että eri kuolinpaikkojen taustalta olisi ollut löydettävissä muitakin tekijöitä. Jatkossa olisi mielenkiintoista selvittää esimerkiksi potilaiden perus- ja välitöntä kuolinsyytä ja katsoa, onko niillä yhteys kuolinpaikkaan.
Toinen keskeinen huomio on, että tulokseemme tukihoitojen vaikutuksesta elossa pysymiseen tulee suhtautua kriittisesti. Ensinnäkään emme huomioineet sairauden etenemistä hidastavan rilutsolilääkityksen (19) esiintyvyyttä. Emme myöskään eritelleet nopeasti ja hitaasti (SOD1-D91A-homotsygoottimuoto) eteneviä tautimuotoja toisistaan. Varsinkin hitaasti etenevälle tautimuodolle on ominaista, että potilaat saattavat pärjätä jopa 10–20 vuotta ilman ylimääräisiä tukihoitoja. Tämä puolestaan voi osaksi selittää, miksi elossaoloajat risteävät Kaplan–Meier-kuvaajissa: ilman tukihoitoja olevat potilaat pysyvät lopulta elossa pidempään kuin tukihoitoja käyttävät. On myös mahdollista, että osan tukihoidot aloitettiin liian myöhään sairauden loppuvaiheessa, jolloin niiden vaikutus elossa pysymiseen jäi olemattomaksi.
Emme myöskään eritelleet erikseen otsa-ohimolohkodementiasta (C9ORF72-geenin toistojaksomutaatio) kärsiviä ja siten tukihoitoihin huonosti sopeutuvia potilaita. Tämä saattaa niin ikään vaikuttaa elossa pysymistä tarkastelevaan tulokseemme. Koska potilaiden ja tukihoitoa käyttävien määrä oli rajallinen, jätimme myös analysoimatta erikseen yhtä tukihoitoa (PEG ja 2PV) käyttävät potilaat.
Kokonaisuutena tuloksestamme ei tule tehdä yksilötasoisia kliinisiä johtopäätöksiä tukihoitojen vaikutuksesta elossa oloon.
Lopuksi
Löydöksemme antaa aihetta kiinnittää huomiota ALS-potilaiden taustatekijöihin elämän loppuvaiheen hoitoa ja hoitopaikkaa suunniteltaessa. Varhaista palliatiivisen hoitokontaktin luomista ja kotisaattohoidon tukemista ei voi liioin korostaa. Kotisaattohoidon rinnalle olisi kuitenkin hyvä suunnitella vaihtoehtoinen tukiosasto, sillä erikoissairaanhoito ei mielestämme ole tarkoituksenmukainen elämän loppuvaiheen hoitopaikka.
Jatkossa olisi tärkeä tutkia, ovatko tekemämme tulokset havaittavissa laajemmalla kansallisella aineistolla.
Waltteri Siirala, Maria Silvoniemi, Eliisa Löyttyniemi, Manu Jokela, Outi Akrén: Ei sidonnaisuuksia.
Jussi P. Posti: Apuraha (Suomen Akatemia).
Tämä tiedettiin
• Amyotrofinen lateraaliskleroosi (ALS) on harvinainen liikehermoja rappeuttava sairaus, johon ei ole parantavaa hoitoa.
• Kansainväliset suositukset suosittavat sairauden moniammatillista hoitoa.
• Ennakoivalla hoitosuunnitelmalla on mahdollista vaikuttaa potilaan kuolinpaikkaan.
Tutkimus opetti
• ALS:iin sairastuneista 80 % menehtyi muualla kuin kotona.
• Kotona tai sairaalassa menehtyneistä valtaosa oli parisuhteessa, kun taas palvelutalossa menehtyneistä valtaosa oli yksinäisiä naisia.
• Saattohoitovaihetta lähestyvä ALS-potilas tulee osata tunnistaa, jotta hoito ehditään järjestää tarkoituksenmukaisessa paikassa.
- 1
- Longinetti E, Fang F. Epidemiology of amyotrophic lateral sclerosis: an update of recent literature. Curr Opin Neurol 2019;32:771–6.
- 2
- Wijesekera LC, Leigh PN. Amyotrophic lateral sclerosis. Orphanet J Rare Dis 2009;4.
- 3
- Logroscino G, Piccininni M. Amyotrophic lateral sclerosis descriptive epidemiology: the origin of geographic difference. Neuroepidemiology 2019;52:93–103.
- 4
- Xu L, Liu T, Liu L ym. Global variation in prevalence and incidence of amyotrophic lateral sclerosis: a systematic review and meta-analysis. J Neurol 2020;267:944–53.
- 5
- Hanhisuanto M, Solje E, Jokela M, Sipilä JOT. Neuroepidemiology Amyotrophic Lateral Sclerosis in Southwestern and Eastern Finland. Neuroepidemiology 2023;57:238–45. https://doi.org/10.1159/000531238
- 6
- Feldman EL, Goutman SA, Petri S ym. Amyotrophic lateral sclerosis. Lancet 2022;400:1363–80.
- 7
- Burkhardt C, Neuwirth C, Sommacal A, Andersen PM, Weber M. Is survival improved by the use of NIV and PEG in amyotrophic lateral sclerosis (ALS)? A post-mortem study of 80 ALS patients. PLoS One 2017;12:e0177555.
- 8
- Cheng HWB, Chan OMI, Chan CHR, Chan WH, Fung KS, Wong KY. End-of-life characteristics and palliative care provision for patients with motor neuron disease. Am J Hosp Palliat Care 2018;35:847–51.
- 9
- Hobson E V, McDermott CJ. Supportive and symptomatic management of amyotrophic lateral sclerosis. Nat Rev Neurol 2016;12:526–38.
- 10
- Andersen PM, Abrahams S, Borasio GD ym. EFNS guidelines on the clinical management of amyotrophic lateral sclerosis (MALS) – revised report of an EFNS task force. Eur J Neurol 2012;19:360–75.
- 11
- Miller RG, Jackson CE, Kasarskis EJ ym. Practice parameter update: the care of the patient with amyotrophic lateral sclerosis: drug, nutritional, and respiratory therapies (an evidence-based review): report of the quality standards subcommittee of the American academy of neurology. Neurology 2009;73:1218–26.
- 12
- Forma L, Aaltonen M, Raitanen J, Anthun KS, Kalseth J. Place of death among older people in Finland and Norway. Scand J Public Health 2020;48:817–24. https://doi.org/10.1177/1403494820944073
- 13
- Sennfält S, Kläppe U, Thams S ym. Dying from ALS in Sweden: clinical status, setting, and symptoms. Amyotroph Lateral Scler Frontotemporal Degener 2023;24:237–45. https://doi.org/10.1080/21678421.2022.2096411
- 14
- Hirvonen OM, Leskelä RL, Grönholm L ym. The impact of the duration of the palliative care period on cancer patients with regard to the use of hospital services and the place of death: a retrospective cohort study. BMC Palliat Care 2020;19:37. https://doi.org/10.1186/s12904-020-00547-8
- 15
- Finne-Soveri H, Malmila M, Kehusmaa S, Jyrkkiö S, Forsius P. Palliatiivisen hoidon ja saattohoidon säädösmuutosten kustannusvaikutusten arviointi: Laskentatyöryhmän raportti. Sosiaali- ja terveysministeriö, Raportteja ja muistioita 2021:21. http://urn.fi/URN:ISBN:978-952-00-5594-3
- 16
- Spataro R, Ficano L, Piccoli F, La Bella V. Percutaneous endoscopic gastrostomy in amyotrophic lateral sclerosis: effect on survival. J Neurol Sci 2011;304:44–8. https://doi.org/10.1016/j.jns.2011.02.016
- 17
- Sarasate M, González N, Córdoba-Izquierdo A ym. Impact of early non-invasive ventilation in amyotrophic lateral sclerosis: a multicenter randomized controlled trial. J Neuromuscul Dis 2023;10:627–37. https://doi.org/10.3233/JND-221658
- 18
- Bourke SC, Tomlinson M, Williams TL, Bullock RE, Shaw PJ, Gibson GJ. Effects of non-invasive ventilation on survival and quality of life in patients with amyotrophic lateral sclerosis: a randomised controlled trial. Lancet Neurol 2006;5:140–7. https://doi.org/10.1016/S1474-4422(05)70326-4
- 19
- Miller RG, Mitchell JD, Moore DH. Riluzole for amyotrophic lateral sclerosis (ALS)/motor neuron disease (MND). Cochrane Database Syst Rev 2012;2012:CD001447. https://doi.org/10.1002/14651858.CD001447.pub3
Background factors affect the palliative care and place of death of ALS patients
Background Amyotrophic lateral sclerosis (ALS) is a rare degenerative motorneuron disease with no curative treatment. The mean life expectance from diagnosis is approximately 2-4 years. The aim of our study was to clarify, where ALS-patients’ end of life (EOL) care was carried out and what factors were associated with the place of death.
Methods In our study we reported the place of death, intimate relationship, sex, age, and the use of noninvasive ventilation (NIV) and percutaneous endoscopic gastrostomy (PEG) among patients who were diagnosed with ALS during 2002-2022.
Results All together 299 patients were diagnosed with ALS and 260 patients died during the 20 years follow up period. 20% of them died at home, 28% at primary ward, 15% in hospital, 13% in specialized hospice care and 21% at sheltered home. 76% of patients who deceased at home and 69% who deceased at hospital had intimate relationship while 74% who died at sheltered home were lonely and mainly female.
Conclusions Most of the ALS-patients died out of home. The intimate relationship, sex, and age might be associated with the place of death. According to our findings it could be recommended to pay attention to these factors when planning the EOL care. Our findings should be ensured with a larger sample size.
Waltteri Siirala, Maria Silvoniemi, Jussi P. Posti, Eliisa Löyttyniemi, Manu Jokela, Outi Akrén